在一个2 L的密闭容器中,加入3 mol A和1 mol B,发生下述反应:
3A(g)+B(g)2C(g)+3D(s),5 min达到平衡时,C的浓度为0.6 mol/L。
(1)达到平衡时,A的转化率为 ,此温度下的平衡常数K= 。
(2)维持容器的温度不变,若缩小容器的体积,则平衡将向 (填“正反应方向移动”“逆反应方向移动”或“不移动”)。
(3)维持容器的体积和温度不变,向密闭容器中加入氦气,达到新平衡时,B、C的浓度之比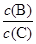 将 (填“增大”、“减小”或“不变”)。
将 (填“增大”、“减小”或“不变”)。
(4)当增加A的浓度,B的转化率 ;若将C分离出来,化学平衡常数 。(填“增大”、“减小”或“不变”)
活性炭可处理大气污染物NO。T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
| 活性炭/mol |
NO/mol |
A/mol |
B/mol |
|
| 起始状态 |
2.030 |
0.100 |
0 |
0 |
| 2 min时 |
2.000 |
0.040 |
0.030 |
0.030 |
(1)2 min内,用NO表示该反应的平均速率v(NO)=______mol·L-1·min-1。
(2)该反应的化学方程式是______;T℃时,它的平衡常数K=9/16,则2 min时反应______(填“是”或“不是”)平衡状态;已知升高温度时,K增大,则该反应为______(填“吸热”或“放热”)反应。
(3)为了提高反应速率和NO的转化率,可采取的措施是______。
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等。
| Q |
R |
||
| T |
W |
(1)T的原子结构示意图是______。用化学方程式表示工业常用冶炼T单质的原理是______。
(2)与W同主族的某元素,其氢化物分子中含有18个电子,该分子中存在的共 价键的类型是______。
(3)元素的非金属性:Q______W(填“强于”或“弱于”),结合方程式简述其原因是______。
(4)甲是R的氧化物,通常状况下呈红棕色。现有一试管甲,欲使元素R全部转化为其最高价氧化物对应水化物,实验步骤:将盛有甲的试管倒扣在水槽中,______。
以丙烯为原料合成高分子纤维P的路线如下: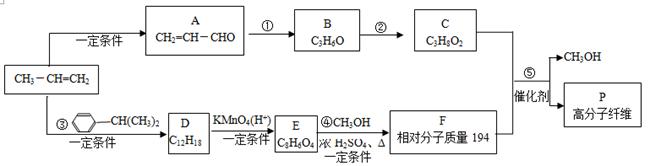
已知:RCOOR'+R"18OH RCO18OR"+R'OH
RCO18OR"+R'OH
(1)①的反应类型是______。
(2)C的核磁共振氢谱显示3个吸收峰,②的化学方程式是______。
(3)③是加成反应,D分子中苯环上的一氯代物只有一种。D的结构简式是______。
(4)④的化学方程式是______。
(5)P的结构简式是______。
氯丁橡胶E(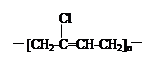 )的合成路线如下:
)的合成路线如下: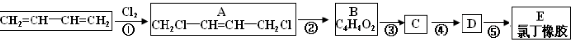
已知: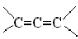 是不稳定结构。
是不稳定结构。
(1)氯丁橡胶中官能团的名称是______。
(2)②的反应条件和无机试剂是______。
(3)若A为反式结构,用结构简式表示A的结构是______。
(4)④的化学方程式是______。
(5)B的同分异构体有多种,写出属于酯类且能发生银镜反应的所有同分异构体的结构简式:______。
A、B、C三种强电解质,它们在水中电离出的离子为Na+、Ag+、NO3-、SO42-、Cl-,在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了10.8克。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”),甲、乙两个烧杯中的电解质分别为 、 (填写化学式)。
(2)计算电极f上生成的气体在标准状况下体积为 L。
(3)写出乙烧杯中的电解反应方程式:。
(4)若电解后甲溶液的体积为10L,则该溶液的pH为 。