在一个体积可变的密闭容器中,通入2molHI气体,在一定条件下建立如下平衡:2HI(g) I2(g)+H2(g);△H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是
I2(g)+H2(g);△H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是
| A.保持容器体积不变,升高温度,混合气体的颜色逐渐变深 |
| B.恒温,恒容,充入一定量氦气(不参与反应),则正反应速率和逆反应速率均增大 |
| C.恒温,缓慢压缩容器,使容器体积恒定为0.2L,一定时间后,测得c(I2)=2.5mol/L |
| D.恒温、恒压,再通入2molHI气体,到达平衡状态后,HI转化率会提高 |
下列措施不符合节能减排的是
| A.大力发展火力发电,解决广东电力紧张问题 |
| B.在屋顶安装太阳能热水器为居民提供生活用热水 |
| C.用石灰对煤燃烧后形成的烟气脱硫,并回收石膏 |
| D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,用做家庭燃气 |
人类探测月球发现,在月球的土壤中含有较丰富的质量数为3的氦,它可以作为未来核聚变的重要原料之一。氦的该种同位素应表示
A. He He |
B. He He |
C.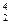 He He |
D. He He |
X元素的1个原子失去2个电子转移到Y 元素的2个原子中去,形成离子化合物Z,下列说法中不正确的是()
元素的2个原子中去,形成离子化合物Z,下列说法中不正确的是()
| A.Z可以电离 | B.Z可以表示为XY2 |
| C.X形成+2价阳离子 | D.Z的电子式为 |
短周期元素A、B、C的位置如图所示,已知B、C两元素所在族序数之和是A元素所在族序数的二倍,B、C两元素的原子序数之 和是A元素的4倍,
和是A元素的4倍,
| A |
||
| B |
C |
则A、B、C依次是()
A.Be、Na、Al B.C、Al、P
C.O、P、ClD.B、Mg、Si
重水 A和普通水
A和普通水 B分别跟足量的金属钠反应,下列叙述正确的是()。
B分别跟足量的金属钠反应,下列叙述正确的是()。
A. A、B质量相等时,产生气体的体积在同温、同压下相等
B. A、B质量相等时,产生气体的质量相等
C. A、B的物质的量相等时,产生气体的体积在同温、同压下相等
D. A、B的物质的量相等时,产生气体的质量相等