银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:
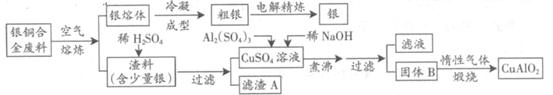
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为 ;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为 。
(2)固体混合物B的组成为 ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 。
(3)完成煅烧过程中一个反应的化学方程式: CuO+ Al2O3 CuAlO2 + ↑。
CuAlO2 + ↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为 mol CuAlO2,至少需要1.0mol•L—1的Al2(SO4)3溶液 L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是 、过滤、洗涤和干燥。
工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)卢布兰芳是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为;
②硫酸钠和焦炭、石灰石反应的化学方程式为_(已知产物之一为CaS);
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。
①图中的中间产物C是_______,D_______。(写化学式);
②装置乙中发生反应的化学方程式为;
(3)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行?。
(4)某工厂用氨制硝酸,再进一步制NH4NO3。已知由NH3制HNO3时产率为88%,由NH3被HNO3的吸收率为98%。则该工厂用100吨氨最多能制硝酸铵吨(计算结果保留整数)。
有机物X(分子式为C4H6O5)广泛存在于许多水果中,尤以苹果、葡萄、西瓜、山楂内为多。经测定该有机物具有下表中所列性质,请根据题目要求填空:
(1)
| X的性质 |
推测X中关于官能团的结论 |
| ①X与足量Na反应产生H2 |
|
| ②X与醇或羧酸在浓硫酸作用下并加热均生成有香味的产物 |
|
| ③在一定条件下X的分子内脱水产物(非环状化合物)可与溴水发生加成反应 |
含—OH |
| ④33.5 g X与100 mL 5 mol·L-1 NaOH溶液恰好中和 |
(2)写出X发生①反应的化学方程式(任写一个)。
(3)在一定条件下X可发生化学反应的类型有。(填序号)
a.水解反应
b.取代反应
c.加成反应
d.消去反应
e.加聚反应
(4)下列物质与X互为同系物的是_______。与X互为同分异构体的是_______(填序号)
A是一种重要的化工原料,它的产量可以衡量一个国家石油化工水平的高低。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
(1)工业上,由石油获得石蜡油的方法是_________,由石蜡油获得A是________变化。
(2)写出A→B的反应方程式:该反应的类型是____________________写出反应B+C→D的化学方程式:____________________________
该反应的类型是。
(3)使1molA与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生完全取代反应,则两个过程中消耗的氯气的总的物质的量是mol
(4)实验室制备D的实验装置图如图所示:收集产物的试管中盛放的液体为;该溶液的作用有:①除掉产物中的和杂质;②
(5)在制备乙酸乙酯过程中,往往加入的乙酸和乙醇的量要比理论计算量多得多,请解析其中可能存在的原因:
①________________________
②________________________
、(1)有机化合物的结构简式可进一步简化,如: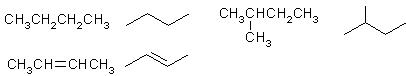
写出下列物质的分子式:
①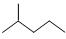 分子式用系统命名法对该有机物进行命名_______________
分子式用系统命名法对该有机物进行命名_______________
② 分子式
分子式
③ 分子式______________
分子式______________
(2)除去下列物质中的杂质(括号内为杂质),填入所用试剂和分离方法。
①乙烯(SO2),试剂,分离方法______________
②苯(溴),试剂,分离方法______________
下表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)A~E中,属于烃的是(填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为。
(3)C催化氧化生成D的化学方程式为。
(4)有机物B具有的性质是 (填序号)。
①无色无味的液体;
②有毒;
③不溶于水;
④密度比水大;
⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是 (用化学方程式说明)。