以乙炔或苯为原料可合成有机酸H2MA,并进一步合成高分子化合物PMLA。
I.用乙炔等合成烃C。
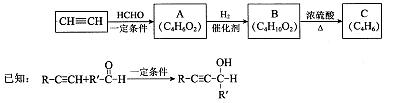
(1)A分子中的官能团名称是 、 。
(2)A的一种同分异构体属于乙酸酯,其结构简式是 。
(3)B转化为C的化学方程式是 ,其反应类型是 。
II.用烃C或苯合成PMLA的路线如下。
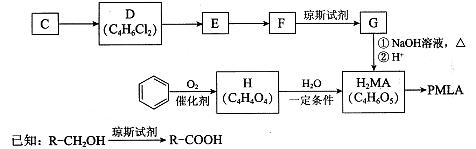
(4)1 mol有机物H与足量NaHC03溶液反应生成标准状况下的C02 44.8L,H有顺反异构,其反式结构简式是 。
(5)E的结构简式是 。
(6)G与NaOH溶液在加热条件下反应的化学方程式是 。
(7)聚酯PMLA有多种结构,写出由H2MA制PMLA的化学方程式(任写一种) 。
(14分)某强酸性溶液X中可能含有NH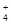 、Fe2+、Al3+、CO
、Fe2+、Al3+、CO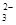 、SO
、SO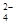 、Cl-、NO
、Cl-、NO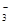 中的若干种。某研究性学习小组为探究溶液X的组成,进行如下实验(其中Y为无色无味的气体):
中的若干种。某研究性学习小组为探究溶液X的组成,进行如下实验(其中Y为无色无味的气体):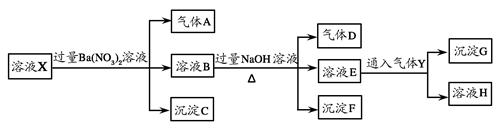
回答下列问题:
(1)溶液X中肯定存在的离子有________。
(2)写出生成气体A的离子方程式__________________。
(3)写出向溶液E中通入少量Y时一定发生的离子方程式_____________。
(4)则溶液中可能存在的离子________________________。
(5)由沉淀F在KOH溶液中与KClO反应可制得一种新型、高效、多功能水处理剂。已知该水处理剂是一种含氧酸盐,取3.96 g该盐溶于水,滴加适量稀硫酸后,再加入0. 04 mol铁粉,恰好完全反应生成Fe2+。向反应后的溶液加入一定量的KOH溶液至刚好将Fe2+沉淀完全,过滤,将沉淀充分加热后得到0.03 mol Fe2O3。将滤液在一定条件下蒸发可得到一种纯净的不含结晶水的含氧酸的正盐(不是复盐)Z,测得其物质的量为0.08 mol。
①Z的化学式为________,水处理剂的摩尔质量为________。
②完成并配平下列方程式:

欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:(系数按顺序填在答题卷上)
用单线桥标出电子转移的方向和数目。
___ C+ ___ KMnO4+ ____ H2SO4→____CO2↑+ ____MnSO4 + ____K2SO4+ ____H2O
(2)焦炭可用于制取水煤气。测得12 g 碳与水蒸气完全反应生成水煤气时,吸收了131.6 kJ热量。该反应的热化学方程式为。
(3)活性炭可处理大气污染物NO。在2 L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
 物质 物质T/℃ n/mol |
活性炭 |
NO |
E |
F |
| 初始 |
2.030 |
0.100 |
0 |
0 |
| T1 |
2.000 |
0.040 |
0.030 |
0.030 |
| T2 |
2.005 |
0.050 |
0.025 |
0.025 |
①请结合上表数据,写出NO与活性炭反应的化学方程式。
②根据上述信息判断,温度T1和T2的关系是(填序号)__________。
a.T1>T2 b.T1<T2 c.无法比较
(4)标准状况下,将4.48LCO2通入200mL 1.5mol/L的NaOH溶液,所得溶液中各离子浓度由大到小的顺序为。
(5)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用 Li2CO3和 Na2CO3的熔融盐混合物作电解质, CO 为负极燃气,空气与 CO2的混和气为正极助燃气,制得在 650 ℃下工作的燃料电池,其阳极反应式:2CO + 2CO32- =4CO2 +4e- 则阴极反应式:_______ ,电池总反应式:
(6)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10—9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10—4mo1/L ,则生成沉淀所需CaCl2溶液的最小浓度为。
(7)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的电离平衡常数K=。(已知:10-5.6=2.5×10-6)。
HCO3-+H+的电离平衡常数K=。(已知:10-5.6=2.5×10-6)。
(14分)硫—碘循环分解水制氢主要涉及下列反应: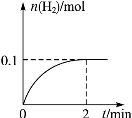
Ⅰ SO2+2H2O+I2===H2SO4+2HI
Ⅱ 2HI H2+I2
H2+I2
Ⅲ 2H2SO4===2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是______。
a.反应Ⅲ易在常温下进行
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程中产生1 mol O2的同时产生1 mol H2
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应
2HI H2+I2,H2物质的量随时间的变化如图所示。0~2 min内的平均反应速率v(HI)=__________。该温度下,H2(g)+I2(g)
H2+I2,H2物质的量随时间的变化如图所示。0~2 min内的平均反应速率v(HI)=__________。该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=______。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则______是原来的2倍。
2HI(g)的平衡常数K=______。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则______是原来的2倍。
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡______移动(填“向左”“向右”或者“不”);若加入少量下列试剂中的______,产生H2的速率将增大。
a.NaNO3 b.CuSO4c.Na2SO4 d.NaHSO3
(4)以H2为燃料可制成氢氧燃料电池。
已知2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1。某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为________。
(8分)晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体结构如右图所示。 随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定精确度也越来越高。现有一简单可行的测定方法,具体步骤如下:①将固体食盐研细,干燥后,准确称取m gNaCl固体并转移到定容仪器A中。②用滴定管向仪器A中加苯,并不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为VmL。回答下列问题:
(1)步骤①中A仪器最好用__________________(填序号)。
| A.量筒 | B.烧杯 | C.容量瓶 | D.试管 |
(2)步骤②中是用酸式滴定管还是用碱式滴定管
(3)经X射线衍射测得NaCl晶胞中最邻近的Na+ 和Cl-平均距离为a cm,则利用上述方法测得的阿伏加德罗常数的表达式为NA=_________。
(4)纳米材料的表面原子占原子数的比例很大,这是它具有许多特殊性质的原因,假设某氯化钠纳米颗粒的形状恰好类似氯化钠晶胞,其大小为氯化钠晶胞大小的8倍,
则这种纳米颗粒的表面原子占总原子数的百分比为_____________(保留一位小数)。
(15分)现有aA、bB、cC、dD、eE、fF五种短周期元素,它们都是生命体不可缺少的重要元素。已知它们的原子序数有如下关系:a+b=c,a+c=d,a+d="e" ,d+e=f,C、E、F都有多种同素异形体。人类已知的化合物中,有一类化合物的种类已超过三千万种,这类化合物中一般都含有A、C两种元素。根据以上信息回答下列有关问题:
(1)元素F的电子排布式:_______________
(2)由A、B、D形成的化合物N和苯互为等电子体,则N的结构式为_____________
(3)A和E按原子个数比1 : 1形成的化合物是______________分子(填极性和非极性)
(4)写出由A、C、D、E四种元素组成的离子化合物和共价化合物的化学式(各写出1种即可) _____________________ 、
(5)在A、C、E三种元素中选择2种或3种元素,组成2种可发生反应的阴离子,请写出该反应的离子方程式:___________________________________________。
(6)B和D按原子个数比1 : 1形成的化合物有两种,一种为质地较软的P,一种为质地坚硬的Q,P的结构和石墨相似,则在P的晶胞中包含_____个B,_____个D,Q的结构和金刚石相似,晶胞边长为361.5pm,则Q的密度是_______g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。