【选修2-化学与技术】
“烂版液”是制印刷锌板时,用稀硝酸腐蚀锌板后得到的“废液”(含有少量的Cl-、Fe3+),某化学兴趣小组拟用“烂版液”制取Zn(NO3)2·6H2O的过程如下: 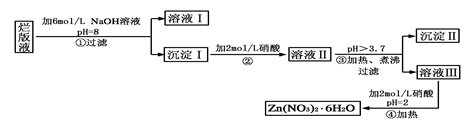
已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂版液”中溶质的主要成分是________(填化学式),若稀硝酸腐蚀锌板产生的气体为N2O,写出稀硝酸腐蚀锌板反应的主要化学方程式______________________。
(2)在操作①中保持pH=8的目的是_________________________________。
(3)沉淀Ⅰ的主要成分是___________________________________________。
(4)操作③中加热、煮沸的目的是___________。此步骤操作的理论依据是_______________。
(5)操作④保持pH=2的目的是_______。此步骤操作中所用的主要仪器是_____ ______。
(1)有下图所示A、B、C、D四种仪器: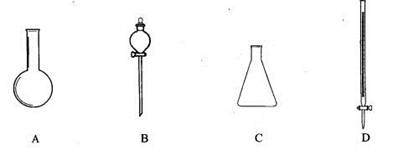
请选择下列仪器名称的序号,填入相应的空格内:
①烧杯②普通漏斗③圆底烧瓶④锥形瓶⑤分液漏斗⑥酸式滴定管
A ______________ B______________C______________D______________
(2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,该同学的操作是错误的,而烧杯的实际质量应为___________g.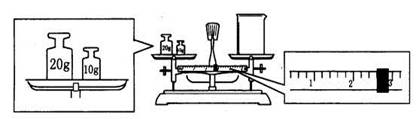
(3)指出下面3个实验中各存在的一个错误:
A_________________,B___________________,C___________________。
有一包白色固体粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成。
②向①的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
③取少量②的溶液滴加稀硫酸,有白色沉淀生成;
④另取少量②的溶液滴加AgNO3溶液,有白色沉淀生成。
(1)根据上述实验现象,判断原粉末的组成成分是(写名称)____________。
(2)写出实验步骤①和③中有关反应的方程式:
________________________________________________________________。
两种液体混合物A和B,已知A、B互溶。且相互不发生化学反应。在常温下,A的沸点为35℃,B的沸点为200℃。请回答下列问题
(1)用蒸馏方法分离物质和提纯混合物必不可少的仪器和用品
(2)当随着温度的升高,哪一种物质先分馏出来?
粗盐提纯中除含有钙离子、镁离子、硫酸根离子等可溶性杂质,还含有泥沙等不溶性杂质。我们食用的精盐是用粗盐提纯而得到的。通过教材中“粗盐提纯”及你做过的该实验回答下列问题:
(1)如何运用最简单的方法检验溶液中有无SO42ˉ离子?________________。
如果有,应该如何除去SO42ˉ离子?_____________________。
(2)在粗盐经过溶解,过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止,请问这步操作的目的是_______________________。
(3)实验室将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:____________________________;
过滤时:____________________________;
蒸发时:____________________________。
某学生设计了三个实验方案,用以检验淀粉的水解情况。
(1)方案甲:
淀粉液 水解液
水解液 中和液
中和液 溶液变蓝。结论:淀粉没有水解。
溶液变蓝。结论:淀粉没有水解。
(2)方案乙:
淀粉液 水解液
水解液 无红色沉淀。结论:淀粉完全没有水解。
无红色沉淀。结论:淀粉完全没有水解。
(3)方案丙:
淀粉液 水解液
水解液 中和液
中和液 有红色沉淀。结论:淀粉已水解。
有红色沉淀。结论:淀粉已水解。
(4)方案丁:
结论:淀粉部分水解。
以上四种方案的设计及结论是否正确?如不正确,请简述理由。