白酒产品中的塑化剂主要源于塑料接酒桶、塑料输酒管、成品酒塑料内盖等。DBP是塑化剂的一种,可由下列路线合成:
已知以下信息:
①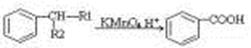
②
(-R1、-R2表示氢原子或烃基)
(1)A的结构简式 ,D的结构简式是 ,D→E的反应类型 。
(2)D和H2 1︰1反应生成E,则E官能团名称为_________,DBP的分子式为 .
(3)由B和E以物质的量比1︰2合成DBP的化学方程式: 。
(4)写出同时符合下列条件的B的所有同分异构体结构简式 。
①能和NaHCO3溶液反应生成CO2 ③能使FeC13溶液发生显色反应
②能发生银镜反应 ④苯环上含碳基团处于对位
(5)写出B与碳酸氢钠溶液反应的方程式 。
写出C生成D的反应的方程式 。
某校兴趣小组对氢氧化钠溶液和稀盐酸混合后的有关问题,进行了如下探究:
Ⅰ.(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发 生反应,设计并完成了如图所示
生反应,设计并完成了如图所示
实验。
X溶液是,滴入的量一般为。
(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应。在盛有氢氧化钠溶液的 试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。
试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。
①写出测定溶液pH的方法:。
②上图中哪个图像符合该同学的记录(填序号)。
(3)你认为甲、乙两位同学的实验中,(填“甲同学”、“乙同学”或“甲、乙两同学”)的实验能充分证明氢氧化钠溶液与盐酸发生了反应,请说明理由:。
Ⅱ.丙同学测出10mL 10%的NaOH溶液和不同体积的10%的盐酸溶液混合过程中,溶液的温度变化见下表(假设两溶液密度相同)。
| 加入盐酸的 体积(  )/mL )/mL |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
| 溶液温度上升 |
5.2 |
9.6 |
12.0 |
16.0 |
18.2 |
16.7 |
15.7 |
14.7 |
13.7 |
就此实验回答:
(4)盐酸和氢氧化钠的反应是(填“吸热”或“放热”)反应。
(5)请在图中绘制出溶液的温 度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。
度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。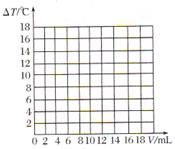
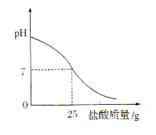
Ⅲ.丁同学为测定标示质量分数为32%的盐酸的实际质量分数,用pH测定仪组成实验装置。实验时先在烧杯中加入20g 40%的氢氧化钠溶液,再逐滴加入该盐酸,pH测定仪打印出加入盐酸的质量与烧杯中溶液的pH关系如图所示。
(6)请以此次测定的结果为依据计算该盐酸的实际质量分数为。
(7)请分析你的计算结果与标签标示的质量分数不一致的可能原因(若一致,此空可不填):。
有关物质存在如图所示转化关系(部分产物已略去)。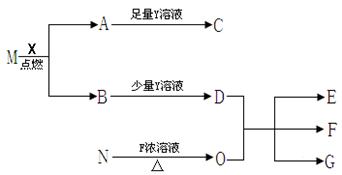
已知A、B是均能使澄清石灰水变浑浊的气体。M为无色液体,常用作有机溶剂,其结构与A相似且为非极性分子。C、E均难溶于水且E难溶于酸。
(1)单质N在X中燃烧可形成一种具有磁性的黑色物质,则构成N的元素在周期表中的位置为。
(2)M的电子式为,Y的化学式为。
(3)①写出离子方程式:A→C
②检验O中阴离子的方法为
(4)将M滴入O溶液中,观察到溶液变浑浊,请推断反应的化学方程式:
。
X、Y、Z三种短周期元素,其单质在常温下都是无色气体,它们的原子序数之和为16。在适当条件下三种单质直接化合,可发生如右图所示变化。已知一个B分子中含有Z元素的原子个数比 C分子中的Z元素的原子个数少一个。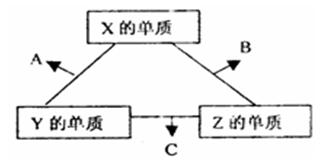
请回答下列问题:
(1)X、Z两元素也可按1:1组合成另一种物质D,D 的电子式为,A与C在一定条件下可生成无污染的物质,请写出该反应的化学方程式
(2)X的单质与Z的单质可制成新型的化学电 源(KOH溶液作
源(KOH溶液作 电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。则:正极通入的物质名称是;负极电极反应式为。
电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。则:正极通入的物质名称是;负极电极反应式为。
(3)X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W溶液吸收生成一种盐。该盐的水溶液pH7(填“大于”、“小于”或“等于”)其原因是(用离子方程式表示):。
(4)已知Y的单质与Z的单质生成C的反应是可逆反应,△H<0。将等物质的量的Y、Z的单质充入一密闭容器中,在适当催化剂和恒温,恒压条件下反应。下列说法中,正确的是(填写下列各项的序号)。
a.达到化学平衡后,再升高温度,C的体积分数增大
b.达到化学平衡时,Y、Z的两种单质在混合气体中的物质的量之比为1:1
c.反应过程,Y的单质体积分数始终为50%
d.达到化学平衡的过程中,混合气体的密度增大
e.达到化学平衡时,正反应速率与逆反应速率相等
上海世博会英国馆——种子圣殿,由六万多根透明的亚克力[其分子式是(C5H8O2)n]杆构建而成。某同学从提供的原料库中选择一种原料X,设计合成高分子亚克为的路线如图所示: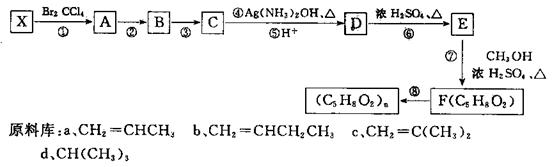
请回答:
(1)原料X是____(选填序号字母),其核磁共振氢谱有____个峰,峰面积之比为。
(2)反应②的条件是____;反应⑧的反应类型是____;
(3)C有多种同分异构体,其中分子中含有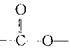 结构的同分异构体有种,请写出其中任意两种的结构简式____、____。D中官能团的名称。
结构的同分异构体有种,请写出其中任意两种的结构简式____、____。D中官能团的名称。
(4)写出⑦的化学方程式。
有E、Q、T、x、z五种前四周期元素,原子序数E<Q<T<X<Z。E、Q、T三种元素的基态原子具有相同的能级,且I1(E)<I1(T)<I1(Q),其中基态E原子占有三个能级且每个能级中电子数目相等,基态Q原子的2p轨道处于半充满状态,X为周期表中前四周期电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)氢元素和E、Q两种元素形成分子式为HEQ的化合物,HEQ分子属于分子(填“极性”或“非极性”),分子中有个σ键。
(2)与分子式为ET互为等电子体的离子是(写出一种即可)。基态Z原子的核外电子排布式____。
(3)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有(写两种)。
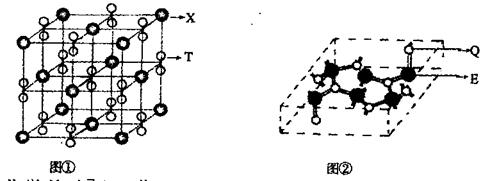
(4)化合物甲由T、X两种元素组成,其晶胞如图①,甲的化学式为。甲与E的最高价氧化物反应的方程式为。
(5)化合物乙的晶胞如图②,乙由E、Q两种元素组成,硬度超过金刚石。
①乙的晶体类型为;②乙的晶体中Q元素原子的杂化方式为。