(14 分) 一氧化碳被广泛应用于冶金工业和电子工业。
⑴高炉炼铁是最为普遍的炼铁方法,相关反应的热化学方程式如下:
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H="a" kJ·mol-1
CO(g)+3Fe2O3(s)=CO2(g)+2Fe3O4(s) △H="b" kJ·mol-1
反应3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)的△H= kJ·mol-1(用含a、b 的代数式表示)。
⑵电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到。
第一步:2CH3OH(g) HCOOCH3(g)+2H2(g) △H>0
HCOOCH3(g)+2H2(g) △H>0
第二步:HCOOCH3(g) CH3OH(g) +CO(g) △H>0
CH3OH(g) +CO(g) △H>0
①第一步反应的机理可以用下图表示:
图中中间产物X的结构简式为 。
②在工业生产中,为提高CO的产率,可采取的合理措施有 。
⑶为进行相关研究,用CO还原高铝铁矿石,反应后固体物质的X—射线衍射谱图如图所示(X—射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。反应后混合物中的一种产物能与盐酸反应生产两种盐,该反应的离子方程式为 。
⑷某催化剂样品(含Ni2O340%,其余为SiO2)通过还原、提纯两步获得镍单质:首先用CO将33.2 g样品在加热条件下还原为粗镍;然后在常温下使粗镍中的Ni与CO结合成Ni(CO)4(沸点43 ℃),并在180 ℃时使Ni(CO)4重新分解产生镍单质。
上述两步中消耗CO的物质的量之比为 。
⑸为安全起见,工业生产中需对空气中的CO进行监测。
①粉红色的PdCl2溶液可以检验空气中少量的CO。若空气中含CO,则溶液中会产生黑色的Pd沉淀。每生成5.3gPd沉淀,反应转移电子数为 。
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其结构如图所示。这种传感器利用原电池原理,则该电池的负极反应式为 。
尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室通过下列方法制取:将MnO2和Li2CO3按4︰1的物质的量比配料,球磨3~5小时,然后升温至600℃~750℃,保温24小时,自然冷却至室温得产品。
(1)保温24小时的目的是____________________________________________________。
(2)写出该反应的化学方程式_________________________________________________。
(3)实验室测定锰酸锂中锰的平均化合价的实验步骤如下:
步骤1:准确称取0.1g左右的尖晶石型锰酸锂试样于锥形瓶中,加入5mL稀硫酸、10.00mL 0.2000mol/L草酸钠(Na2C2O4)标准溶液,于80℃水浴加热溶解;
步骤2:待试样全部溶解,立即用浓度为0.2000mol/L的高锰酸钾溶液滴定至终点;
步骤3:计算样品得电子的物质的量n;
步骤4:将溶液中Mn2+氧化为Mn3+,再用硫酸亚铁铵标准溶液滴定,记录实验数据,计算出样品中Mn元素的质量为m;
步骤5:将实验步骤1-4重复2次。
已知反应: 2Mn3++C2O42-=2Mn2++2CO2↑;Mn4++C2O42-=Mn2++2CO2↑
2MnO4-+5C2O42-+16H+="2" Mn2++10 CO2↑+8H2O
①步骤2中,为判断滴定终点,_________(填“需要”或“不需要”)加入指示剂。
②步骤4中,滴定时盛放硫酸亚铁铵标准溶液的玻璃仪器是___________________。
③请用样品得电子的物质的量n和样品中Mn元素的质量m来表示样品中Mn元素的化合价=_____。
实验室有NH4HCO3和NaHSO3的干燥粉状混合物,某兴趣小组为测定其中NH4HCO3的含量,设计了用在混合物中加酸的实验方法来测定其质量分数。回答以下问题:
⑴化学小组主要选用了下列药品和仪器进行实验。(图中每种仪器装置只选用了一次,铁架台等固定仪器未画出)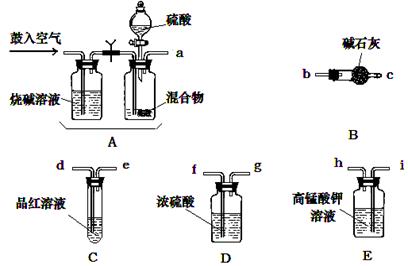
请按气流由左向右的方向,仪器连接顺序是(填仪器的接口字母a、b...)
a→→→→→ f →g → →。
⑵实验开始,混合物加酸前,A装置需要鼓入空气,作用是;加酸后A装置再次鼓入空气的作用是。
⑶ E装置的作用是。
⑷实验中,若C瓶中溶液褪色,则测定结果可能会偏(填“高”或“低”)。为了确
保实验中C瓶溶液不褪色,若取样品的质量为m g,实验前 E中所装 a mol·L-1的KMnO4
溶液体积(V)不少于mL。
⑸若混合物样品质量为13.1g,充分作用后碱石灰增重4.4g,则混合物中NH4HCO3的质
量分数为。
⑹从定量测定的准确性考虑,该套装置还应作进一步的改进是。
可能用到的相对原子质量:H~1 C~12 N~14 O~16 Na~23 S~32
实验室用下列仪器组装一套蒸馏石油的装置,并进行蒸馏得到汽油和煤油。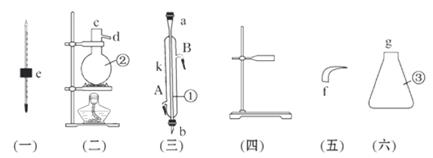
(1)写出下列仪器的名称:
①__________________;②___________________;③_________________。
(2)将以上仪器按从左到右顺序,用字母a、b、c……进行连接:
e接();()接();()接()接()
(3)①仪器的A口是__________,B口是__________。
(4)蒸馏时,温度计水银球应在______________________(位置)。
(5)在②中注入原油后,加几片碎瓷片的目的是_________________。
过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用。某学生为了验证这一实验,以足量的大理石、足量的盐酸和过氧化钠样品为原料,制取O2,设计出如下实验装置: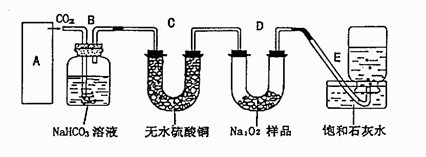
(1)A中制取CO2 的装置,应从下列图①、②、③中选哪个图:
B装置的作用是,C装置内可能出现的现象是。
(2)二氧化碳和过氧化钠反应的化学方程式为,
(3)为了检验E中收集到的气体,在取出集气瓶后,如何检测。
(4)若乙中的石灰水出现出现轻微白色浑浊,请说明原因:。
实验室欲配制0.5 mol·L-1的NaOH溶液500 mL有以下仪器:①烧杯②100 mL量筒③1 000 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)
(1)配制时,必须使用的仪器有(填代号) ,还缺少的仪器是
(2)需称量 g烧碱固体,固体应放在 中称量。
(3)配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却。其正确的操作顺序为 。
(4)在配制过程中,其他操作都正确,下列操作会引起误差偏高的是 。
| A.未洗涤烧杯、玻璃棒 |
| B.未等NaOH溶液冷却至室温就转移到容量瓶中 |
| C.容量瓶不干燥,含有少量蒸馏水 |
| D.定容时俯视标线 |
E、摇匀后液面下降,补充水