人类的生产和生活都离不开金属。
(1)金属的应用非常广泛。
①汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和________性。
②铁是生产和生活中使用最多的金属,下列关于铁的叙述不正确的是________。
| A.铁生锈时生成四氧化三铁 | B.表面涂漆以防止铁生锈 |
| C.铁制品应放置于干燥的环境中 | D.应及时回收废弃的的铁制品 |
金属活动性顺序有重要的应用。铝、铜、铁为日常生活中常见的金属,某化学兴趣小组的同学在探究铝、铜、铁三种金属的有关性质时,进行了如下图实验: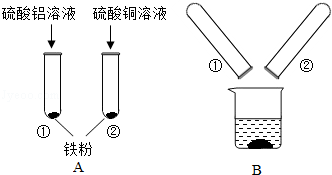
在A实验中发生反应的化学方程式为________________,反应类型为________。将A实验结束后①、②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,一段时间后过滤,滤渣中的物质所有可能的组成为________,滤液中的溶质可能为________(填写以下序号)。
①Al2(SO4)3②Al2(SO4)3、FeSO4③Al2(SO4)3、Fe2(SO4)3
④FeSO4、CuSO4⑤Al2(SO4)3、FeSO4、CuSO4
钛(Ti)是一种重要的航天金属材料.某学习小组对三种金属Ti、Al、Cu的金属活动性顺序进行探究.过程如下:
提出假设:a.Ti金属活动性比Al强 b.Al金属活动性比Cu强
查阅资料:钛能与盐酸反应.
实验设计:同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
操作分析:三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是
A.除去氧化膜,利于直接反应
B.使表面光亮,易观察现象
C.使反应金属温度相同,易反应
| 金属 |
Ti |
Al |
Cu |
| 与盐酸反应现象 |
反应缓慢 |
反应剧烈 |
无明显现象 |
实验现象,实验结论:
(1)原假设中不正确(填“a”、“b”或“a、b”).
(2)三种金属的金属活动性由强至弱的顺序为。
结论应用:能否用铝制容器来盛装波尔多液(含硫酸铜),(填“能”或“否”),理由是。
过氧化钠是化学中常见的一种药品,它是浅黄白色颗粒粉末.在空气中吸收水分和二氧化碳。易溶于水,与水中能发生反应生成氢氧化钠和过氧化氢,方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能分解放出氧气。
(1)区分水和过氧化氢的实验方法是:,发生的反应方程式是:.
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究.
提出问题:什么导致溶液先变红再褪色?
猜想与假设:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”.
实验与结论:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
| 实验步骤 |
实验现象 |
实验结论 |
| 取少量稀氢氧化钠溶液于试管中,滴加1﹣2滴酚酞试液,变红后观察现象 |
溶液依然为红色 |
讨论交流:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分.(化学试卷总分不超过60分)
猜想3:
方案3:
| 实验步骤 |
实验现象 |
实验结论 |
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答
| 编号 |
操作 |
实验现象 |
| ① |
分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴等浓度 FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. |
试管A中不再产生气泡;试管B中产生的气泡量增大. |
| ② |
另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 |
试管A、B中均未明显见到有气泡产生. |
(1)过氧化氢分解的化学方程式为.
(2)实验①的目的是.
实验中滴加FeCl3溶液的目的是.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是 (用实验中提供的试剂).
(4)某同学在50mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积与反应时间的关系如图1所示,则A、B、C三点所表示的瞬时反应速率最慢的是.
(5)催化剂是化学反应前后均未改变的一类化学物质.
(6)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:
①定性分析:如图甲可通过观察,定性比较得出结论.有同学提出将FeCl3改为更为合理,其理由是.
②定量分析:用图乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是.
英国科学家法拉第在《蜡烛的故事》系列讲座中,对蜡烛燃烧所涉及的知识进行了全面介绍.生产蜡烛的主要原料是石蜡和少量的硬脂酸添加剂等有机物,现在让我们一起对蜡烛原料的组成元素进行探究.
(1)写出C不完全燃烧的化学方程式:.
[提出问题]生产蜡烛的原料中主要有哪些元素?
[假设与猜想]主要原料为有机物,猜想:
(2)①一定有元素;②可能还有氢元素和氧元素.
[实验设计]据上述三种元素的猜想制订实验方案.
实验一:如图1所示,在蜡烛火焰上方放置一块洁净、干燥的玻璃片,一会儿观察到玻璃片上生成一些细小的水珠.
实验二;如图2所示,在蜡烛火焰上方罩一个内壁附着有澄清石灰水的烧杯,观察现象.
[证据与结论](3)实验一,观察到玻璃片上有细小水珠时,说明原料中一定存在(填元素符号).实验二,观察到烧杯内壁附着的,则猜想①成立.
[分析与交流](4)实验一和实验二获得的证据均不能证明原料中一定存在 元素,因为.
(5)写出C的两条化学性质.
某校化学兴趣小组将用剩的过氧化氢溶液倒入放有生锈铁钉的废液缸中,发现产生了大量的气泡,经检验此气体为氧气.根据学过的知识初步判断,是生锈铁钉中的某种物质加快了过氧化氢的分解,那么究竟是哪种物质加快了过氧化氢的分解速率?请你参与他们的研究,分享和体验探究实验的快乐.
[猜想与假设]
甲同学:铁钉表面的氧化铁加快了H2O2的溶液分解.
乙同学:铁钉里的加快了H2O2的溶液分解.
[设计方案和实验] 完成下列表格
| 实验方案 |
实验现象 |
结论 |
| 方案一:向盛有10mL 5% H2O2溶液的试管中 加入2g氧化铁粉末,将一根带火星的木条放 在试管口,观察现象. |
甲同学结论成立. |
|
| 方案二:向盛有10mL 5% H2O2溶液的试管中加入粉末,将一根带火星的木条放在试管口,观察现象. |
乙同学结论. (填“成立”或“不成立”) |
[讨论交流] 丙同学认为“方案一”只能说明Fe2O3加快了H2O2溶液的分解,并不能说Fe2O3就一定是催化剂.你是否支持丙同学的观点?,如果要证明氧化铁是催化剂,就要设计一个实验来证明,这个实验的设计原理是.
(提示:下面小题若答对将奖励4分,但化学总分不超过60分.)
[反思与评价] 丁同学仔细观察“方案二”中一直没有现象的试管,过了一段时间后发现试管中也产生了气体,丁同学对此现象进行深入思考和分析,得出可能的原因,你能想出其中的原因吗?。