(12分) (1)水的电离平衡曲线如图所示,若A点表示25 ℃时水的电离达平衡时的离子浓度,B点表示95 ℃时水的电离达平衡时的离子浓度。则95℃时0.1 mol·L-1的NaOH溶液中,由水电离出的 c(H+)=________mol·L-1,Kw(25 ℃)______Kw(95℃)(填“>”、“<”或“=”)。25 ℃时,向水的电离平衡体系中加入少量NH4Cl 固体,对水的电离平衡的影响是________(填“促进”、“抑制”或“不影响”)。
(2)25℃时,在0.1L 0.2 mol·L-1的HA溶液中,有0.001mol的HA电离成离子,则该溶液的pH= ,电离度为 。
(3)电离平衡常数是衡量弱电解质电离程度强弱的量(已 知如右表数据)。向NaCN溶液中通入少量CO2,所发生反应的化学方程式为 。
| 化学式 |
电离平衡常数(25 ℃) |
| HCN |
K=4.9×10-10 |
| H2CO3 |
K1=4.3×10-7、K2=5.6×10-11 |
已知两个羟基同时连在同一个碳原子上时结构是不稳定的,它将发生脱水反应,例如:CH3CH(OH)2→CH3CHO +H2O,现有分子式为C9H8O2Br2的物质M,已知E的化学式为C7H5O2Na,A的相对分子质量为46,在一定条件下可发生下列一系列反应: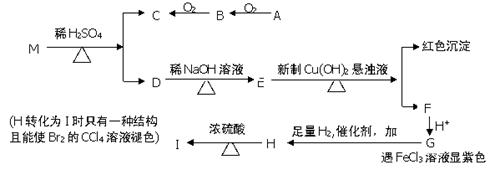
请回答下列问题
(1)B中官能团的名称,A的核磁共振氢谱有个吸收峰;G→H的反应类型。
(2)M的结构简式
(3)写出下列反应的化学方程式
①E→F ②H→I
(4)同时符合下列条件的G的同分异构体的结构简式有种,写出其中一种
| A.分子中含有苯环 | B.能发生水解反应 | C.能发生银镜反应 | D.与FeCl3溶液反应显紫色 |
A,B,C,D,E,F,G是元素周期表前四周期元素,原子序数依次增大,根据下表提供的有关信息,回答下列问题
| 元素 |
相关信息 |
| A |
所有单质中密度最小 |
| B |
形成化合物种类最多的元素 |
| D |
基态原子中只有3个能级,有2个未成对电子 |
| E |
短周期中原子半径最大 |
| F |
第三周期中电负性最大的元素 |
| G |
最外层只有一个电子,内层填满电子 |
(1)F元素原子的价电子排布式,B,C,D三元素第一电离能由大到小顺序为(填元素符号)
(2)写出由A,B,C,D四种元素形成的一种简单的既能与酸反应又能与碱反应的化合物
(3)写出由元素E、F形成化合物的水溶液用惰性电极电解的离子方程式
(4)由A,B,C形成的三原子化合物中含有σ键个,π键个
(5)已知下列反应:
①G(s) + 1/2O2 (g) =" GO" (s) ;△H=-157.0 KJ/mol
②B(s) + O2 (g) = AO2(g) ;△H=-393.5 KJ/mol
写出单质B与足量GO 反应的热化学方程式
将红热的黑色固体单质甲投入显黄色的溶液乙中剧烈反应产生混合气体A,A在常温下不与空气作用。现有如下变化关系:
气体A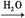
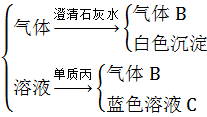
试推导:
(1)甲为 ,乙为 ,丙为 。
(2)混合气体A的主要成分是 。
(3)气体B为 ,蓝色溶液C溶质为 。
(4)甲与乙反应的化学方程式是 。
在浓硝酸中放入铜片:
(1)开始反应的离子方程式为 ,
实验现象为 。
(2)若铜有剩余,则反应将要结束时的离子方程式为 。
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是 。
(4)若将12.8 g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况下)。则所消耗硝酸的物质的量是 。
某金矿曾发生硝酸泄漏事故。由于浓硝酸易挥发且不稳定,事故发生时,有大量黄色、并有刺激性气味的烟雾产生。消防官兵到达后,立即对泄漏硝酸进行处理(抛撒大量白色粉末等),及时地消除了事故带来的危害。
(1)请用化学方程式解释烟雾呈黄色的原因:
。
(2)消防官兵向泄漏的硝酸抛撒的白色粉末可能是 。
| A.生石灰 | B.烧碱 | C.食盐 | D.石膏 |
(3)若图中的E物质代表硝酸,请完成下列反应: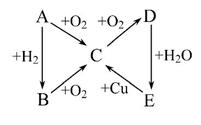
①B→C的化学反应方程式: ;
②D→E的化学反应方程式: ;
③E→C的离子反应方程式: 。