在陶瓷工业生产中往往由于陶土里混有氧化铁而使产品质量受到影响。解决的方法是:将陶土和水一起搅拌,使陶土粒子直径达到10-9—10-7 m,然后插入两根电极,接通直流电源,这时正极聚集____________________,负极聚集_______________________,从而除去氧化铁。理由是____________________。
X.Y.Z代表原子序数依次增大的三种短周期元素,在周期表中三种元素的位置相邻,且质子数之和为30。
(1)X.Y.Z三种元素能否位于同一族(填“能”或“否”),
理由是。
(2)若X.Y.Z三种元素中有金属元素,则X是(填元素符号),而Z与过量NaOH溶液反应的离子方程式为。
(3)若X.Y.Z均为主族非金属元素,由X和Y组成的化合物 A中,X和Y元素的质量比为7:16,则A可以为色的(填化学式)。
A中,X和Y元素的质量比为7:16,则A可以为色的(填化学式)。
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。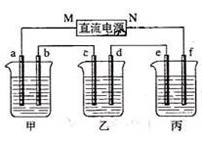
⑴、接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①、电源的N端为▲极;
②、电极b上发生的电极反应为▲;
③、列式计算电极b上生成的气体在标准状况下的体积为▲;
④、电极c的质量变化是▲g;
⑤、电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液▲;乙溶液▲;丙溶液▲。
⑵、如果电解过程中铜全部析出,此时电解▲(填“能”或“否”)继续进行,理由是▲。
用右图所示装置进行中和热测定实验,请回答下列问题:
⑴、大小烧杯之间填满碎泡沫塑料的作用是▲,从实验装置上看,图中缺少的一种玻璃仪器是▲。
⑵、使用补全仪器后的装置进行实验,取50mL0.25mol/LH2SO4溶液与 50mL0.55 mol/L NaOH溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃。已知中和后生成的溶液的比热容c为 4.18J/ (g·℃),溶液的密度均为1g/cm3。通过计算可得中和热
△H= ▲, H2SO4与NaOH反应的热化学方程式 ▲。
⑶、实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 ▲(填“相等”、“不相等”),所求中和热 ▲(填“相等”、“不相等”);若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会 ▲。(填“偏大”、“偏小”、“不受影响”)
⑷、若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为ΔH 1,则ΔH1与ΔH的关系为:ΔH 1 ▲ΔH(填“<”、“>”或“=”),理由是 ▲。
金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。 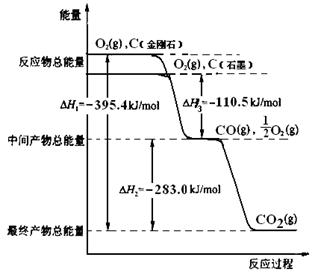
⑴、等量金刚石和石墨完全燃烧▲(填“金刚石”或“石墨”)放出热量更多,表示石墨燃烧热的热化学方程式▲。
⑵、在通常状况下,金刚石和石墨▲(填“金刚石”或“石墨”)更稳定,写出石
墨转化为金刚石的热化学方程式▲。
⑶、12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量▲。
图1是氯碱工业中离子交换膜电解槽示意图,其中离子交换膜是“阳离子交换膜”,它有一特殊的性质——只允许阳离子通过而阻止阴离子和气体通过。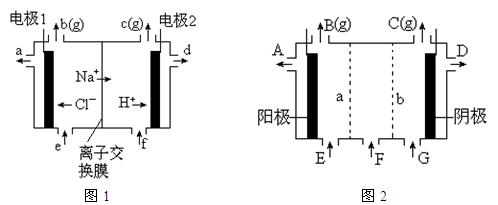
⑴、工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为▲,▲。
⑵、如果粗盐中SO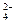 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO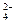 ,该钡试剂可以是▲。
,该钡试剂可以是▲。
A.Ba(OH)2B.Ba(NO3)2C.BaCl2
⑶、为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为▲。
A.先加NaOH,后加Na2CO3,再加钡试剂
B.先加NaOH,后加钡试剂,再加Na2CO3
C.先加钡试剂,后加NaOH,再加Na2CO3
⑷、电解后得到的氢氧化钠溶液从▲口流出,b口排出的是▲气体,电极1应连接电源的
▲极(填“正”或“负”极);理论上讲,从f口加入纯水即可,但实际生产中,纯水中要加入一定量的NaOH溶液,其原因是▲。
⑸、图2是根据氯碱工业中离子交换膜技术原理,设计的电解Na2SO4溶液生产NaOH和H2SO4溶液的装置。请回答:
①、a为▲(填“阳”、“阴”)离子交换膜。
②、阳极的电极反应式是▲。
③、从D、E口流出或流进的物质的化学式分别为▲,▲。