实验室配制480mL 0.5 mol·L-1的NaCl溶液,有如下操作步骤:
①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液小心转入500 mL容量瓶中;
③继续向容量瓶中加蒸馏水至液面距离刻度l~2 cm处,改用胶头滴管小心滴加适量的蒸馏水后停止滴加;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞紧,充分摇匀。
请填写下列空白:
(1)实验操作步骤的正确顺序为(填序号) ____ ___。
(2)实验中用托盘天平称取NaCl晶体的质量是____ ____。
(3)上述操作步骤③中定容时,如果加水超过了刻度线,应如何处理?____ ____。
(4)若实验时出现如下情况,对所配溶液浓度将有何影响?(选填“偏高”、“偏低”、“无影响”)
①定容时,仰视刻度线: ____ ___。
②移液后,未洗涤烧杯和玻璃棒: ____ ___。
③容量瓶中原来有少量水: 。
(12分)据图回答下列问题:
Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是___________,负极反应式为:_________________。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________(填Mg或Al),总反应化学方程式为____________________________________。
Ⅱ、由Al、Cu、浓硝酸组成原电池,其正极的电极反应式为_____。
Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
(1)该电池工作时,b通入的物质为_______,c通入的物质为______。
(2)该电池负极的电极反应式为:_______
(3)工作一段时间后,当12.8 g甲醇完全反应生成CO2时,有______________NA个电子转移。
某课外兴趣小组对H2O2的分解速率做了如下实验探究。
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)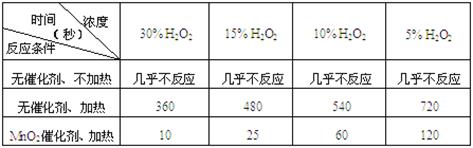
①该小组在设计方案时,考虑了浓度、a:、b:等因素对过氧化氢分解速率的影响。
②从上述影响H2O2分解速率的因素a和b中任选一个,说明该因素对该反应速率的影响:。
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试。测定结果如下:
| 催化剂(MnO2) |
操作情况 |
观察结果 |
反应完成所需的时间 |
| 粉末状 |
混合不振荡 |
剧烈反应,带火星的木条复燃 |
3.5分钟 |
| 块状 |
反应较慢,火星红亮但木条未复燃 |
30分钟 |
①写出H2O2发生的化学反应方程式 _____________________。
②实验结果说明催化剂作用的大小与_________________有关。
(11分)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
(1)科学家提出由CO2制取C的太阳能工艺如图所示。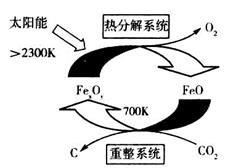
①若“重整系统”发生的反应中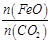 =6,则FexOy的化学式为______________。
=6,则FexOy的化学式为______________。
②“热分解系统”中每分解l mol FexOy,转移电子的物质的量为________。
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-53.7kJ·mol-1
CH3OCH3(g)+H2O(g)=2CH3OH △H2=+23.4kJ·mol-1
则2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H3=kJ·mol-1
CH3OCH3(g)+3H2O(g) △H3=kJ·mol-1
①一定条件下,上述合成二甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是_____(填代号)。
a.逆反应速率先增大后减小
b.H2的转化率增大
c.反应物的体积百分含量减小
d.容器中的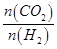 值变小
值变小
②在某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的转化率如下图所示。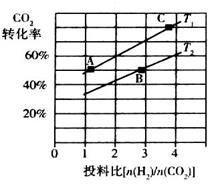
T1温度下,将6 mol CO2和12 mol H2充入2 L的密闭容器中,5 min后反应达到平衡状态,则0~5 min内的平均反应速率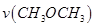 =______;KA、KB、KC三者之间的大小关系为______________。
=______;KA、KB、KC三者之间的大小关系为______________。
Ⅰ.图甲是一定的温度和压强下N2和H2反应生成1 mol NH3过程中能量变化示意图,请写出工业合成氨的热化学方程式(ΔH的数值用含字母Q1、Q2的代数式表示):。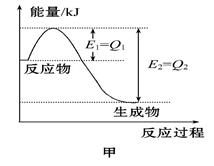
Ⅱ.(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应,
已知:N2(g)+3H2(g)="=" 2NH3(g) ΔH="-92.4" kJ·mol-1,
2H2(g)+O2(g)====2H2O(l) ΔH="-571.6" kJ·mol-1,
则2N2(g)+6H2O(l)="=" 4NH3(g)+3O2(g) ΔH=;
(2)饮用水中的NO3-主要来自于NH4+。已知在微生物的作用下, NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如图乙: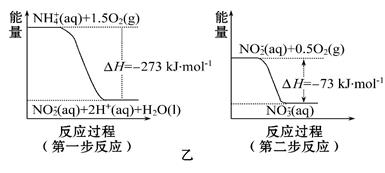
1 mol NH4+全部被氧化成NO3-的热化学方程式为。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍;A的一种原子中,质量数与质子数之差为零。D元素的原子最外层电子数为m,次外层电子数为n;E元素的原子L层电子数为m+n,M层电子数为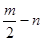 。请回答下列问题:
。请回答下列问题:
(1)D元素在周期表中的位置是_____________________;
(2)写出一个E和D形成的化合物与水反应的离子方程式_______________________;
(3)已知:甲+ H2O → 丙+ 丁。若甲是由N和Cl元素组成的化合物,其分子结构模型如图所示,丙具有漂白性。则甲中Cl元素的化合价是,丁与H2O有相同的电子总数,则丁的化学式为。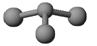
(4)与D同主族上下相邻的元素M、N,原子电子层数M>N>D,三种元素氢化物沸点由大到小的顺序是(填写化学式)。
(5)写出B与D在高温下完全反应后生成物的电子式___ __,结构式___