(12分)过氧化钙晶体[CaO2·8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液。广泛应用于环境杀菌、消毒等领域。
★过氧化钙晶体的制备
工业上生产CaO2·8H2O的主要流程如下: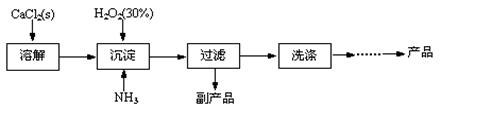
(1)用上述方法制取CaO2·8H2O的化学方程式是 。
(2)沉淀时常用冰水控制温度在10℃以下和通入过量的NH3,其可能原因分别是
① ;② 。
★过氧化钙晶体含量的测定
准确称取0.3000g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol·L-1 H2SO4,用0.0200 mol/LKMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O
(3)滴定终点观察到的现象为 。
(4)根据表1数据
表1. KMnO4标准溶液滴定数据
| 滴定次数 |
样品的质量/g |
KMnO4溶液的体积/mL |
|
| 滴定前刻度/mL |
滴定后刻度/mL |
||
| 1 |
0.3000 |
1.02 |
24.04 |
| 2 |
0.3000 |
2.00 |
25.03 |
| 3 |
0.3000 |
0.20 |
23.24 |
计算产品中CaO2·8H2O的质量分数(写出计算过程):
金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态Ni原子的价电子(外围电子)排布式为;
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式、;
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③ 、④HCHO,其中碳原子采取sp2杂化的分子有(填物质序号),HCHO分子的立体结构为形;
、④HCHO,其中碳原子采取sp2杂化的分子有(填物质序号),HCHO分子的立体结构为形;
(4)Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiOFeO(填“<”或“>”);
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示。该合金的化学式为;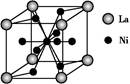
元素H、C、N、O、F都是重要的非金属元素,Fe、Cu是应用非常广泛的金属。
(1)Fe元素基态原子的核外电子排布式为。
(2)C、H元素形成的化合物分子中共有16个电子,该分子中σ键与π键的个数比为。
(3)C、N、O三种元素的第一电离能由大到小的顺序为(用元素符号表示)。
(4)在测定HF的相对分子质量时,实验测得值一般高于理论值,其主要原因是。
(5)C、N两元素形成的化合物C3N4形成的原子晶体,结构类似金刚石,甚至硬度超过金刚石,其原因是。
(6)如图为石墨晶胞结构示意图,该晶胞中含有C原子的个数为。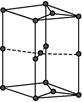
物质的转化关系如图所示(有的反应可能在水溶液中进行)。其中甲为淡黄色固体化合物,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化,用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成。请回答下列问题:
(1)写出甲的电子式:。
(2)写出反应Ⅰ的化学方程式:。
(3)A溶于水得到溶液X,在25 ℃下,将a mol·L-1的X与b mol·L-1的G溶液等体积混合,溶液显中性,则所得溶液中离子浓度由大到小的顺序为,
用含a和b的代数式表示出该混合溶液中X的电离平衡常数。
(4)工业上采用的一种污水处理方法是:保持污水的pH在5.0~6.0之间,通过如图装置处理污水。
①电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:Ⅰ.;Ⅱ.。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分Y物质参加循环(见上图)。Y物质的化学式是。
如图表示常见元素单质及化合物相应关系,某些生成物已略去。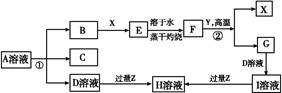
已知:反应①为氯碱工业的基础反应;X、Y为常见金属,Z为形成酸雨的主要成分。请回答下列问题:
(1)D的电子式;H为(填化学式)。
(2)完成下列方程式:
①空气中含量最高的气体与C反应的化学反应方程式;
②反应②的化学反应方程式;
③足量B通入H溶液的离子反应方程式。
过氧化氢(H2O2)是一种无色黏稠液体,它的水溶液俗称双氧水,呈弱酸性,常用作无公害的消毒杀菌剂和漂白剂等。
(1)下列说法正确的是。
| A.过氧化氢分子中既有极性键又有非极性键 |
| B.H2O2与H2O互为同素异形体 |
| C.34 g H2O2中含有的阴离子数为NA |
| D.实验室可以利用过氧化氢制取氧气 |
(2)H2O2是一种二元弱酸,请写出它的第二步电离方程式:。
(3)将H2O2溶液加入酸性FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式:。
(4)某厂工业废水中含有一定量氯气,为了除去氯气,常加入H2O2作脱氯剂,写出该反应的化学方程式:。