中和反应是中学化学中重要的学习内容,其在日常生活和工农业生产中有广泛的应用。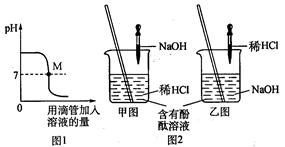
(1)上图表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH的变化曲线。
请从曲线图中获取信息,回答下列问题:
①图1图象表示盐酸和氢氧化钠溶
液发生反应过程中溶液的pH变化。进行该反应的实验操作是按照图2中的_______(填甲或乙)图所示进行的。
②曲线上M点表示盐酸和氢氧化钠溶液反应的情况是_______。
③向烧杯中倾倒20 g(滴有2滴酚酞试液)质量分数为4.0%的氢氧化钠溶液,振荡,再逐滴滴入质量分数为7.3%的稀盐酸,边滴边振荡,直至溶液刚好变为_______色为止,共用去稀盐酸10 g,则反应后溶液中溶质质量分数为_______。要使反应后的溶液变成20℃时的饱和溶液,需要加入氯化钠固体的质量是_______g(结果精确到0.1 g)。已知:20℃时氯化钠的溶解度为36.0 g。
(2)为证明中和反应是放热反应,某小组进行了如图所示的实验操作: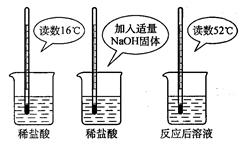
根据图示实验,甲同学认为:NaOH与稀盐 酸发生的中和反应是放热反应。乙同学认为:甲同学得出这个结论的依据不科学,理由是__________。
(3)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、D、E的五只烧杯中各装入36.5 g溶质质量分数分别为5%、10%、15%、20%、25%的盐酸,再向上述五只烧杯中分别加入40 g 20%的氢氧化钠溶液,最后测量其温度,数据记录如下: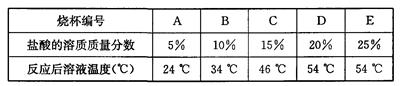
实验结论:影响该中和反应放出热量多少的因素是_______。
地球上的金属资源广泛地存在于地壳和海洋中,工业上主要是从含有金属元素并有开采价值的矿石中提炼金属。
(1)赤铁矿在自然界中储藏丰富,其主要成分的化学式是。
(2)磁铁矿的主要成分是
。在
中存在两种不同价态的铁离子,其中1/3是
,2/3是
。请写出
与盐酸反应的化学方程式。
(3)工业上主要采用高炉炼铁,常用到的原料有铁矿石、焦碳、石灰石和空气。其中,焦碳的作用是。(仅答一点)
(4)由于铁的氧化物中
和
均为黑色,实验室用
还原
得到的铁中是否会含有
和
,某同学设计了下列探究实验。
资料:
溶液与铁发生的反应是2
,但
溶液不与
、
反应;含有
的盐溶液遇到
溶液时变成红色,利用该反应可检验
的存在。
【提出问题】
还原
得到黑色产物的成分是什么?
【猜想】
猜想l:
猜想2:
和
;
猜想3:
和
;猜想4:。
【实验探究】限选试剂:
、盐酸、澄清石灰水、
溶液、
溶液。
| 实验操作 |
实验现象 |
实验结论 |
| Ⅰ取少量黑色产物加入到装有足量
溶液的烧杯中,充分反应后过滤,对过滤所得固体用蒸馏水洗涤。 |
黑色固体部分溶解。 |
猜想2和4都 不成立。 |
| Ⅱ,,. | 黑色固体全部溶解,溶液 不变红色。 |
|
| Ⅲ另取少量黑色产物装入玻璃管中,通入
,一段时间后加热,并将反应后的气体通入装有一定量的的烧杯中。 |
。 |
猜想l不成立, 猜想3成立。 |
如图是某研究性学习小组进行CO2与NaOH溶液反应的探究实验装置.
【查阅资料】水的沸点与气体压强有关,气体压强小,沸点低;气体压强大,沸点高.
【实验探究】实验步骤如下:
步骤①:如图所示,锥形瓶A盛满CO2气体,锥形瓶B盛有96%以上但未沸腾的热水,烧杯中加入同样温度的热水(起保持锥形瓶B中水温恒定的作用).
步骤②:取2支注射器,一支抽取20mL水,另一支抽取20mL浓NaOH溶液.
步骤③:将注射器中20mL水注入锥形瓶A中,振荡后观察,锥形瓶B中的热水没有沸腾.
步骤④:取下盛水的注射器,再将盛20mL浓NaOH溶液的注射器迅速连接到锥形瓶A上,注入该溶液并振荡,观察到明显的现象.
请回答下列问题:
(1)实验开始前,依上图连接好装置(锥形瓶A、B和烧杯均未盛装物质),将一支空注射器连接到锥形瓶A上,并将其活塞缓慢向上拉,几秒钟后松手,观察活塞是否复位,这个操作的目的是 .
(2)锥形瓶A中CO2与NaOH溶液反应的化学方程式是 .
(3)步骤④锥形瓶B中产生的明显现象是 ;产生明显现象的原因是 .
实验室常用的干燥剂"碱石灰"是氧化钙和固体氢氧化钠的混合物,易与空气中的水蒸气和二氧化碳反应而变质。某同学对一瓶久置的碱石灰进行了如下探究:
【猜想与假设】
猜想一:没有变质,只含有氧化钙和氢氧化钠;
猜想二:部分变质;
猜想三:完全变质,含有和。
则氢氧化钠变质的化学反应方程式是。
【进行实验】
实验如下图所示:
【解释与结论】
由操作②的现象判断:猜想三(填"成立"或"不成立");由操作⑤⑥的现象判断滤液中含有,由此判断猜想一不成立,得出结论。
【反思与评价】实验室中碱石灰应该保存。
实验小组同学向盛有2
稀硫酸的试管中加入2
氢氧化钠溶液,未观察到明显现象。
【提出问题】两者是否发生了化学反应?
【实验探究】将盛有上述实验混合液的试管标为①,如图甲。
小华:测得实验所用稀硫酸的
<7,试管①中溶液
>7。于是得出结论:。
小敏:取两支试管,编号为②和③,分别加入稀硫酸和试管①中溶液各2
,逐滴滴加
溶液至过量,实验过程与现象如图乙,由此他得出了与小华一样的实验结论。
【反思评价】小军认为小敏在实验设计中存在不够严密的地方,请帮他指出:。
【交流讨论】试管③中的溶液中有哪些溶质?同学们分析了两位同学的实验过程,一致认为没有
,其理由是。在此基础上,同学们提出了二种推理:
推理1:含有
、
和
推理2:含有 、
正确的是推理(选填"1"或"2")。
像科学家一样做科学
--探究胡萝卜汁对过氧化氢分解的催化作用
体育课上,小华不慎擦伤了皮肤,她用过氧化氢溶液对皮肤进行消毒时,惊奇地发现有嘶嘶的响声,并产生大量气泡。
小华通过查阅文献获得以下信息:
信息Ⅰ:人体皮肤细胞中存在一种叫做过氧化氢酶的物质,能加快过氧化氢分解反应的速率。
信息Ⅱ:胡萝卜汁等植物细胞中也含有过氧化氢酶。
信息Ⅲ:酶是动植物体内活细胞产生的具有催化作用的生物大分子,其催化作用受温度影响。
信息Ⅳ:在没有催化剂时,60℃以下,温度对过氧化氢的分解基本没有影响。
请你在小华探究的基础上,完成以下探究活动。
(1)胡萝卜汁对过氧化氢的分解是否有催化作用?
请完成下表中的实验报告(实验步骤中应包括使用的仪器、药品和实验过程)。
| 实验步骤 |
实验现象 |
实验结论 |
| 胡萝卜汁对过氧化氢的分解有催化作用。 反应的化学方程式 |
(2)温度如何影响胡萝卜汁的催化作用?
药品:
过氧化氢溶液、新鲜胡萝卜汁、不同温度的水(
、
、
、
)。
仪器:
试管
支,
烧杯
只、
量筒、秒表、温度计、刻度尺。
实验:如图所示,用提供的仪器和药品,按如下步骤进行实验:
①两支试管中分别盛有胡萝卜汁和3%过氧化氢溶液;
②将①中的试管放入盛有
水的烧杯中,恒定试管及反应物的温度;
③
以后,把过氧化氢溶液倒入装有胡萝卜汁的试管中,稍微振荡,使胡萝卜汁跟过氧化氢溶液均匀混合;
④将③中的试管放回原烧杯,恒温
;
⑤用刻度尺测量试管中泡沫状混合物的高度;
⑥按上述步骤进行实验,分别测定
、
、
时泡沫状混合物的高度。
每个温度下的实验重复
次,取平均值,得到如下数据:
| 实验编号 |
反应物的温度 |
混合恒温6min时,泡沫的高度(cm) |
| A |
||
| B |
||
| C |
||
| D |
请回答下列问题:
①为了测定实验准确性,该实验过程中还需要控制的条件有。
②请你在下面的直角坐标系中,绘制出泡沫的高度随温度变化而变化的曲线。
(要求:需表示出横坐标和纵坐标表示的数量级单位)
③关于温度对胡萝卜汁的催化作用的影响,你的结论是。