由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。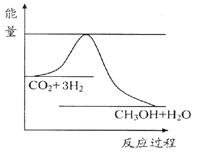
(1)关于该反应的下列说法中,正确的是 。(填字母)
A.△H>0,△S>0 B.△H>0,△S<0 C.△H<0,△S<0 D.△H<0, △S>0且在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(2)该反应平衡常数K的表达式为 。
(3)下列情况不能说明该反应一定达到平衡的是
A.混合气体的平均平均相对分子质量不变 B.混合气体的压强不变
C.单位时间内生成3mol H—H键,同时生成2 mol H—O键
D.混合气体中c (CO2) : c (H2) =" 1" : 3
(4)温度降低,平衡常数K (填“增大”、“不变”或“减小”)。
(5)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2)为 mol·L-1·min-1, CO2和H2的转化率比是 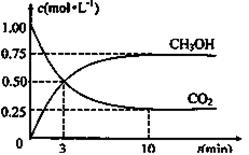
(6)下列措施中能使(5)题中n(CH3OH)/n(CO2)增大的有 。(填字母)
A.升高温度 B.加入催化剂 C.将H2O(g)从体系中分离
D.充入He(g),使体系总压强增大 E.再充入1molCO2和3molH2
(7)若在另一个密闭容器中充入1 mol CO2和3 mol H2,保持压强不变,并使初始体积与题中容器体积相等,且在相同的温度下进行反应,达到平衡时该容器中的CO2的体积百分数 ________(5)题中的CO2的体积百分数。(“>”或“<”或“=”,下同)
(8)若为两个容积相同的密闭绝热容器,现向甲容器中充入1 mol CO2(g)和3 molH2(g),乙容器中充入1mol CH3OH(g)和1 mol H2O(g),在相同的温度下进行反应,达到平衡时,甲容器内n(CH3OH) 乙容器内n(CH3OH)。
请根据所学化学知识回答下列问题:
(1)氯化铁溶液蒸干并灼烧后得到的固体物质的化学式是________。
(2)在浓度均为0.1 mol/L的①CH3COONH4②NH4HSO4③NH3.H2O④(NH4)2SO4四种溶液中,NH4+浓度由大到小的顺序为________(用代号表示)。
(3)25时,某浓度的CH3COONa溶液呈碱性的原因是________(用离子方程式表示),溶液中所有离子的浓度由大到小的顺序是________。
(4)某温度下,蒸馏水的pH = 6,氢氧化物R(OH)2的Ksp = 1×10-13,则R2+沉淀完全时,溶液的pH为_______。
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气的燃烧热值高,H2(g) +1/2 O2(g) = H2O (g)△H =" -241.8" kJ·mol-1
| 化学键 |
H-H |
O=O |
O-H |
| 键能(kJ·mol-1) |
X |
496.4 |
463 |
请根据相关数据计算:H-H的键能X = ________kJ·mol-1。
(2)根据现代工业技术可以用H和CO反应来生产燃料甲醇,其反应方程式如下:
CO2(g) + H2(g) = H2O + CH3OH(g)△H =" -49.00" kJ·mol-1
一定温度下,在体积为1 L的密闭容器中充入1.00 mol CO2和3.00 mol H2,测得CO2和CH3OH的浓度随时间变化如图所示。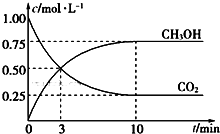
①能说明该反应已达平衡状态的是________(填代号)。
A.CO2在混合气体中的体积分数保持不变
B.单位时间内每消耗1.2 mol H2,同时生成0.4 mol H2O
C.混合气体平均相对分子质量不随时间的变化而变化
D.反应中H2O与CH3OH的物质的量浓度比为1:1,且保持不变
②从反应开始到平衡的平均反应速率v(H2) = ________,达到平衡时氢气的转化率为________。
③该温度下的平衡常数为________(小数点后保留2位)。
④下列的条件一定能加快反应速率并且提高H2转化率的是________(填代号)。
A.升高反应温度
B.缩小容器的体积
C.保持容器体积不变,充入稀有气体
D.保持容器体积不变,充入CO2气体
填写计算结果:
(1)含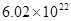 个分子的CO中,
个分子的CO中, 。
。
(2)
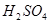 的
的 =。
=。
(3)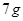
 在标准状况下的
在标准状况下的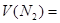 。
。
(4)5L
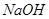 溶液中所含
溶液中所含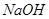 的
的 。
。
(5) 某二价金属氯化物(
某二价金属氯化物(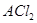 )中含有
)中含有 ,则A的相对原子质量=。
,则A的相对原子质量=。
印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”生成CuCl2和FeCl2,其反应的化学方程式:Cu + 2FeCl3 ═ CuCl2 + 2FeCl2
(1)请在上式中标出电子转移的方向和数目。
(2)上述反应中的氧化剂是:。
(3)写出FeCl3的电离方程式:。
(4)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是(填序号)
| A.氯气 | B.铁 | C.双氧水 | D.稀硫酸 |
能源短缺是人类社会面临的重大问题,利用化学反应可实现多种形式的能量相互转化。请回答以下问题:
(1)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程。已知反应N2(g)+3H2(g) 2NH3(g)△H=-93 kJ·mol-1。试根据表中所列键能数据,计算a 的数值为kJ/mol。
2NH3(g)△H=-93 kJ·mol-1。试根据表中所列键能数据,计算a 的数值为kJ/mol。
| 化学键 |
H-H |
N-H |
N≡N |
| 键能/kJ·mol-1 |
436 |
a |
945 |
(2)甲醇是一种可再生能源,具有广泛的开发和应用前景。已知在常压下有如下变化:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =a kJ/mol
②H2O(g)=H2O(l)ΔH =b kJ/mol
写出液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式:。
(3)可利用甲醇燃烧反应设计一个燃料电池。如下图1,用Pt作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。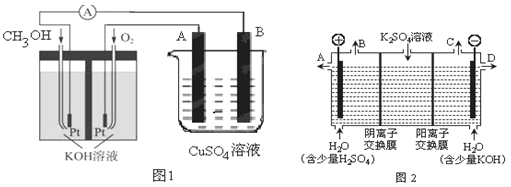
①写出燃料电池正极的电极反应式。
②若利用该燃料电池提供电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是极(填“A”或”B”);当铁件的质量增重6.4g时,燃料电池中消耗氧气的标准状况下体积为L。
(4)如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图2装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾(电解槽内的阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)。
①该电解槽的阳极反应式为,单位时间内通过阴离子交换膜的离子数与通过阳离子交换膜的离子数的比值为。
②从出口D导出的溶液是(填化学式)。