(15分)下图中各物质均由常见元素(原子序数≤20)组成。已知A、B、K为单质,且在常温下A和K为气体,B为固体。D为常见的无色液体。I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生。J是一种实验室常用的中性干燥剂也常作为冬天道路的融雪剂。它们的相互转化关系如右图所示(图中反应条件未列出)。请回答下列问题: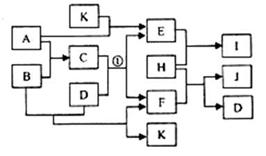
(1)I的电子式为 ;
(2)反应①的化学方程式为 ;
(3)E物质与氧气在催化剂的条件下发生反应的化学方程式为 ;
(4)E的水溶液与H的水溶液按物质的量2:1混合后,溶液中离子浓度大小关系为 ;
(5)X分子含有的元素与E相同,分子内原子个数比为1:2,在空气中燃烧的产物为D和A,写出X做燃料电池(20%-30% KOH为电解质)的负极反应方程式 ;实验室制备X的方法之一是将Cl2与NaOH反应产物之一与E反应,写出该反应离子反应方程式 。
(4分)氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为;
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1)△H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O△H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式;
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。回答下列问题:
⑴ Y在元素周期表中的位置为________________。
⑵上述元素的最高价氧化物对应的水化物酸性最强的是_______________(写化学式),非金属气态氢化物还原性最强的是__________________(写化学式)。
⑶ Y、G的单质或两元素之间形成的化合物可作水消毒剂的有___________(写出其中两种物质的化学式)。
⑷ X2M的燃烧热ΔH=-a kJ·mol-1,写出X2M燃烧反应的热化学方程式:___。
⑸ ZX的电子式为___________;ZX与水反应放出气体的化学方程式__________________。
已知1mol CO气体完全燃烧生成CO2气体,放出283KJ热量,1mol氢气完全燃烧生成液态水放出286KJ热量,1mol CH4气体完全燃烧生成CO2气体和液态水放出890KJ热
(1)写出H2燃烧热的热化学方程式。
(2)若1mol CH4气体完全燃烧生成CO2气体和水蒸汽,放出热量890KJ(填“=”、“>”“<”)
(3)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,则放出热量(Q)的取值范围是。
(4)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,且CO2和H2O物质的量相等,则放出热量(Q)的取值范围是。
依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。
则表示甲醇燃烧热的热化学方程式为_____________________________________;
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量。______________________________;
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量_________________________________。
(4)肼(N2H4)和NO2是一种双组分火箭推进剂。两种物质混合发生反应生成N2和H2O(g),已知8g气体肼在上述反应中放出142kJ热量,其热化学方程式为。
A、B、C、D、E 5瓶透明溶液,分别是HCl 、BaCl2、NaHSO4、Na2CO3、AgNO3溶液中的一种。
①A 与B反应有气体生成② B与C反应有沉淀生成③C与D反应有沉淀生成④D与E反应有沉淀生成⑤A与E反应有气体生成
⑥在②和③的反应中生成的沉淀是同一种物质B是_________D是_________(均填化学式)