(8分)
痛风是关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:
① HUr(尿酸,aq)  Ur―(尿酸根,aq)+H+(aq) (37℃时,Ka =4.0×10-6)
Ur―(尿酸根,aq)+H+(aq) (37℃时,Ka =4.0×10-6)
② NaUr(s)  Ur―(aq)+Na+(aq)
Ur―(aq)+Na+(aq)
(1)37℃时,1.0L水中可溶解8.0×10-3mol尿酸钠,此温度下尿酸钠的Ksp为
(2)关节炎发作大都在脚趾和手指的关节处,这说明温度降低时,反应②的Ksp (填“增大”、“减小”或“不变”),生成尿酸钠晶体的反应是 (填“放热”或“吸热”)反应。
(3)37℃时,某病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3mol/L,其中尿酸分子的浓度为5.0×10-4mol/L,该病人尿液的c(H+)为 mol/L。
A、B、C、D、E分别为(NH4)2SO4、NH4Cl 、NaCl 、Na2SO4、Ba(OH)2五种溶液中的某一种,把它们两两混合:
(1)A和B混合产生白色沉淀,加热,无明显变化;
(2)B和C混合产生白色沉淀,加热,产生使湿润红色石蕊试纸变蓝的气体;
(3)B和E混合无明显变化,加热,产生使湿润红色石蕊试变蓝的气体。
根据以上现象,判断A、B、C、D、E各为什么物质(写物质名称)。
A:、B:、C:、
D:、E:。
氨气极易溶于水,其水溶液显_________(酸性、中性、碱性)。氨气和氯化氢在空气中相遇时,可以看到的现象是__________。
有一瓶无色气体,可能含有CO2,HCl,HBr,SO2 中的一种或几种气体,将气体通入适量氯水中,得到无色透明的溶液,继续向该溶液中加入少量的BaCl2溶液和盐酸,有白色沉淀产生。则原气体中一定含有__________,肯定不含有__________。
如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质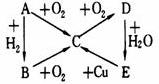
当A是气体单质时,B是______,C是_____,E是______。
浓硫酸在下列用途和现象中所表现的性质是(用编号填写)
| A.沸点高、难挥发 | B.酸性 | C.吸水性 | D.脱水性 E、强氧化性 |
| 用途或现象 |
体现浓硫酸的性质 |
| (1)浓硫酸使蓝矾变成白色 |
|
| (2)浓硫酸使木条变黑 |
|
| (3)浓硫酸制HCl |
|
| (4)浓硫酸与铜片共热 |
|
| (5)浓硫酸与木炭共热产生气体 |