世界上每年因锈蚀而报废的金属设备和材料,高达产量的20%~40%,某实验小组对铁的燃烧和锈蚀进行如下探究
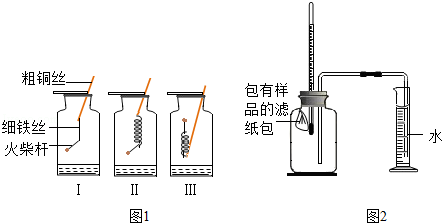
探究一:铁丝燃烧
如图1所示,取3根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端系上粗铜丝,另一端系一根火柴杆,点燃火柴杆待快燃尽时,分别插入充满氧气的集气瓶中,观察到:观察到:Ⅰ、Ⅱ中铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比I中的更剧烈;Ⅲ中铁丝没有燃烧.
(1)集气瓶中加入少量水的作用:.
(2)为什么Ⅲ中铁丝不能燃烧.
(3)分析Ⅱ中铁丝燃烧比Ⅰ中更剧烈的原因.
探究二:铁粉腐蚀的条件
如图2所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进广口瓶(容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
| 序号 |
样品 |
量筒起始 读数/mL |
量筒最终 读数/mL |
所需时间 /min |
| 1 |
1g铁粉、0.2g碳和10滴水 |
100 |
72 |
约120 |
| 2 |
l g铁粉、0.2g碳、10滴水和少量 | 100 |
72 |
约70 |
| 3 |
|
\ |
\ |
\ |
(4)金属腐蚀的过程实际上就是金属元素化合价(填"升高"或"降低")的过程.
(5)实验①和②说明NaCl可以(填"加快"或"减慢")铁锈蚀的速率.
(6)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是(填"放热"或"吸热")过程.
(7)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成是.
(8)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是%(精确到小数点后1位),试分析该实验结果出现误差的原因(写任意一条即可)
根据下列三组实验回答问题。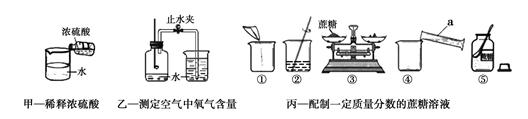
(1)图中仪器a的名称是;三组实验都用到的玻璃仪器是。
(2)指出甲实验中不正确的操作。
(3)乙实验中,燃烧匙中装入的药品应为,其反应的实验现象是。
(4)丙实验中,正确的操作顺序为(填序号):⑤→→→→ ②。
通过半年的化学学习,你对化学实验有了一些认识,请你解答下列问题:
(1)在电解水的实验中,两电极相连的玻璃管上方产生的气体是和,两者的体积比约为,这个实验证明了水是由组成。该反应的化学方程式为。
(2)根据下图所示实验装置回答下列问题: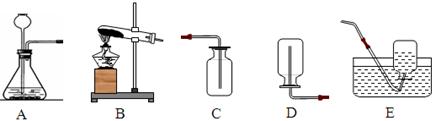
①用氯酸钾和二氧化锰混合加热制取O2应选用的发生装置(填序号,下同)____;若用高锰酸钾加热制取O2该装置还需做的一点改动是;用过氧化氢溶液和二氧化锰混合制取O2应选用_________;制取H2应选用__________;
制取CO2应选用_______,反应的化学方程式为。 ②收集O2可选用________, 理由是; 收集CO2应选用。(3).过滤操作中的要点常简记为“一贴二低三靠”,请你解释“三靠”的具体含义:。
“三靠”:①,② ,
③。
指出下面实验室用高锰酸钾制取氧气的装置图中的三处错误: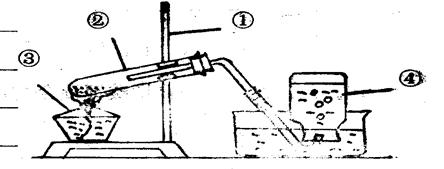
a.
b.
c.
(5分)某兴趣小组做以下实验探究分子有运动。请回答实验中的有关问题。
(1)实验Ⅰ:在盛有少量蒸馏水的小烧杯中滴入2 ~ 3滴酚酞试液,再向其中滴加浓氨水。由实验得出的结论有
。
⑵ 实验Ⅱ(如图甲所示):烧杯B中的现象是;产生这一现象的原因是。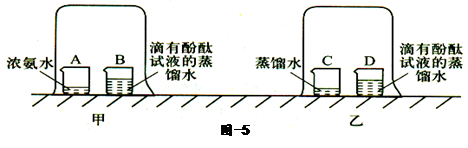
⑶ 为使实验结论准确可靠,兴趣小组成设计实验Ⅲ(如图乙所示)作为对比实验。你认为有无必,理由是。
过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解成氧气和水。分液漏斗可以通过调节活塞控制液体滴加速度。回答下列问题:
⑴分液漏斗中应放入的物质是,锥形瓶中应放入的物质是。
⑵要收集一瓶纯净的氧气应选择上图中的装置(填字母)
⑶某同学在观察到锥形瓶内有大量气泡时,开始用C装置收集氧气,过一断时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃。其原因是。
⑷若实验时用此法代替高锰酸钾加热制氧气,优点是(填序号)
A.生成物中只有氧气 B.不需加热 C.需加热
⑸装置A中反应剧烈,据此提出实验安全注意事项是( )
A.控制液体的滴加速度 B.用体积小的锥形瓶 C.加热反应物