(18分)0.80 g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
请回答下列问题:
(1)试确定200 ℃时固体物质的化学式______。
(2)取270 ℃所得样品,于570 ℃灼烧得到的
主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为___________________;把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为_____,其存在的最高温度是________;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为____________________________________________________________;
(4)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)= mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1 mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是 mol·L-1。
锂—空气电池能够提供相当于普通锂离子电池l0倍的能量,因此它是最有前途的电池技术。下图是锂—空气电池放电和充电时的工作示意图。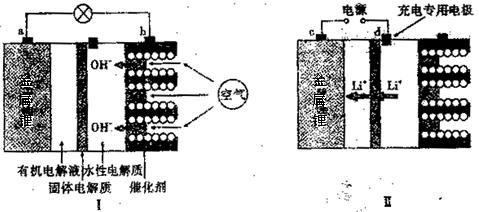
(1)图I中电极a是极。
(2)用锂一空气电池电解100mL 0.5mol/L CuSO4溶液,当电池中消耗1.4g Li时,在阴极会析出g铜。
(3)电池中间的固体电解质(含阳离子交换膜)能阻止H2O、N2、O2等物质的通过,防止Li和这些物质反应。Li和水在常温下发生反应的化学方程式为。
(4)当给图Ⅱ中的锂空气电池充电时,d极应接电源的极,该电极的电极反应式为。
物质间有下列转代关系: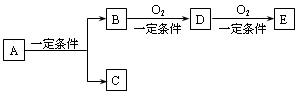
(1)若C是可用于自来水消毒的气体,D、E是氧化物,D转化为E时增加氧的质量是D的质量的25.8%,则A是(写化学式)并写出A在一定条件下生成的C的化学方程式。
(2)若E是酸酐,且为无色易挥发的晶体,A为气态氢化物,则A与D反应生成B的化学方程式为。
(3)若C是水,B是无氧化合物,B在同系物中是相对分子质量最小的化合物;工业上用B与C在催化剂条件下制取A,A为常见的一种燃料。E能使紫色石蕊试液显红色,则由D生成E的反应类型为 。A、B、D、E中能与水形成氢键而易溶于水的是(写结构简式)
如右图所示,晶体硼的基本结构单元都是由硼原子组成的正二十面体,这个多面体中含有20个等边三角形和一定数目的顶角,每个顶角上各有1个原子。



 (1)这个基本结构单元由个硼原子组成,
(1)这个基本结构单元由个硼原子组成,
 共含有个B—B键。
共含有个B—B键。


 (2)假设将此基本结构单元的每个顶角按一定比例且同等
(2)假设将此基本结构单元的每个顶角按一定比例且同等
 程度地削去(切点不重合),可得到另一个多面体,则此多面体含
程度地削去(切点不重合),可得到另一个多面体,则此多面体含
 个五边形,个六边形。若再设此多面体的每个交点处有一个碳
个五边形,个六边形。若再设此多面体的每个交点处有一个碳
 原子,这样就构成了碳元素形成的一种单质分子,此分子的分子式为。
原子,这样就构成了碳元素形成的一种单质分子,此分子的分子式为。
(1)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
NaBiO3+ MnSO4+ H2SO4===Na2SO4+ Bi2(SO4)3+ NaMnO4+ H2O
①上述反应中还原产物是,若有2mol氧化剂在该反应中被还原,则生成的MnO4-被还原为Mn2+时,能将molHCl氧化成Cl2;
②写出NaBiO3固体溶于浓盐酸产生黄绿色气体的化学反应方程式。
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(S)+2H+(aq)="==" Cu2+(aq)+H2(g) ΔH=64.39kJ·mol-1
2H2O2(L)===2H2O(L)+O2(g) ΔH=-196.46kJ·mol-1
H2(g)+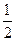 O2(g)===H2O(L) ΔH=-285.84kJ·mol-1
O2(g)===H2O(L) ΔH=-285.84kJ·mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 。
取一定质量的Al粉和一定质量的某种铁的氧化物混合进行铝热反应,两者恰好完全反应。若在反应后混合物中加入足量的稀硫酸,产生H2的体积为V1L,另取相同质量的Al粉,加入足量稀硫酸,产生H2的体积为V2L(V1,V2均在标况下测定),则V2:V1=4:3。另取相同质量的铁的氧化物,加入盐酸溶解,消耗盐酸的物质的量为2.4mol 。则:(1)写出铝热反应方程式(以FexOy表示铁的氧化物)
_______________________________________________________________________。
(2)此铁的氧化物的化学式为_________。
(3)铝粉的物质的量为____________。