乙炔与乙烯类似,在催化剂(10%硫酸和5%硫酸汞的水溶液)的作用下,也可以与等物质的量的水发生加成反应。
(1)已知当羟基和双键碳原子直接相连,呈烯醇结构不稳定,会转化为羰基化合物: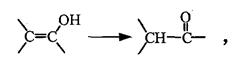
则乙炔和水加成的化学方程式是 。
用如下装置完成乙炔和水的加成反应,加成产物收集在D装置中。(省略部分加热和夹持仪器)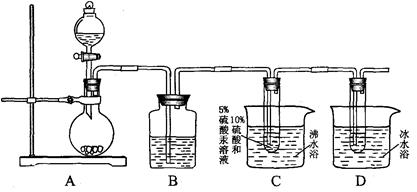
①实验室制备乙炔的化学方程式是 。
②A装置制出的乙炔有难闻的气味,为除去这些杂质,装置B中盛放的试剂是 。
③C装置采用沸水浴的作用是 (填字母)。
a.便于控温,使受热均匀 b.加热反应物,提高化学反应速率 c.蒸出生成物
(3)为检验加成产物中的官能团,选择的药品是 (填字母)。
a.金属钠 b.10%氢氧化钠溶液 c.2%硫酸铜溶液
d.2%硝酸银溶液 e.饱和碳酸钠溶液
检验官能团的实验中,发生反应的化学方程式是 。
已知:X、Y、Z、R四种短周期元素原子序数依次增大,X的气态氢化物水溶液呈碱性,Y原子的L层电子数是K层电子数的3倍,Z和R的单质在一定条件下与铜反应生成Cu2Z和CuR2,请根据要求填空。
(1)画出X的原子结构示意图。R最高价氧化物对应水化物的化学式为。
(2)Y、Z、R三种元素中原子半径最大的是(用元素符号表示)。
(3)X气态氢化物与Z的最高价氧化物对应水化物反应生成的产物中所含化学键的类型为;检验该产物中阳离子的实验方法是。
(4)R的单质通入到澄清石灰水中反应的离子方程式为。
Fe2O3具有广泛的用途。甲同学阅读有关资料得知:在高温下煅烧FeCO3可以得到Fe2O3。为了进一步验证此结论,他做了如下实验:
| 实验步骤 |
实验操作 |
| Ⅰ |
取一定质量的FeCO3固体置于坩埚中,高温煅烧至质量不再减轻,冷却至室温 |
| Ⅱ |
取少量实验步骤I所得固体放于一洁净的试管中,用足量的稀硫酸溶解 |
| Ⅲ |
向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红 |
由此甲同学得出结论:4FeCO3+O2 2Fe2O3+4CO2
2Fe2O3+4CO2
(1)写出实验步骤Ⅲ中发生反应的离子方程式__________________________________。
(2)乙同学提出了不同的看法:煅烧产物可能是Fe3O4,因为Fe3O4也可以溶于硫酸,且所得溶液中也含有Fe3+。于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+。他需要选择的试剂是____________(填序号)。
a.氯水 b.氯水+KSCN溶液 c.K3[Fe(CN)6](铁氰化钾溶液)
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分。你认为丙同学持此看法的理由是____________。
(4)丙同学进一步查阅资料得知,煅烧FeCO3的产物中的确含有+2价铁元素。于是他设计了另一种由FeCO3制取Fe2O3的方法:先向FeCO3中依次加入试剂:稀硫酸、________ (填试剂名称)和氨水;再_________(填操作名称),灼烧,即可得到Fe2O3。
(5)工业上用氧化还原滴定法测菱铁矿中FeCO3的质量分数,通过控制样品的质量,使滴定时消耗KMnO4溶液体积为c mL,对应菱铁矿中FeCO3的质量分数为c%,可以简化计算。某同学取含FeCO3 c%的菱铁矿a g,用足量稀硫酸溶解后,再用0.0 200 mol·L-1的酸性KMnO4溶液滴定(KMnO4被还原成Mn2+),最终消耗KMnO4溶液c mL。假定矿石中无其他还原性物质,则所取菱铁矿的质量a=__________g。(FeCO3的摩尔质量为116 g·mol-1)
第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态。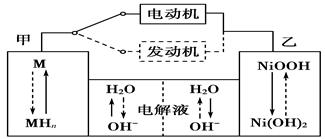
(1)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。镍氢电池充放电原理示意如图,其总反应式为H2+2NiOOH 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,甲电
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,甲电
极周围溶液的pH________(填“增大”“减小”或“不变”),该电极的电极反应_________。
(2)Cu2O是一种半导体材料,可通过如图所示的电解装置制取,电解总反应式为
2Cu+H2O Cu2O+H2↑,阴极的电极反应式是_____________________。
Cu2O+H2↑,阴极的电极反应式是_____________________。
用镍氢电池作为电源进行电解,当电池中有1 mol H2被消耗时,Cu2O的理论产量为______g。
(3)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的________腐蚀。为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,该方法叫 ________。
已知单质硫在通常条件下以S8(斜方硫)的形式存在,而在蒸气状态时,含有S2、S4、S6及S8等多种同素异形体,其中S4、S6和S8具有相似的结构特点,其结构如下图所示: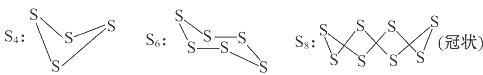
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)。反应过程和能量关系可用下图简单表示(图中的ΔH表示生成1 mol含硫产物的数据)。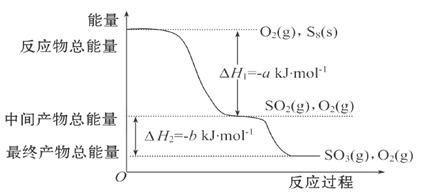
(1)写出表示S8燃烧热的热化学方程式_____________________。
(2)写出SO3分解生成SO2和O2的热化学方程式_________________________。
(3)若已知SO2中硫氧键的键能为d kJ·mol-1,O2中氧氧键的键能为e kJ·mol-1,则S8分子中硫硫键的键能为___________。
已知五种短周期元素的原子序数大小顺序为C>A>B>D>E, A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出E和B形成的化合物分子含非极性共价键的结构式:____________________;
写出A、B、E形成的化合物的电子式:______________。
(2)比较A、B、C三种离子的半径大小_________________(用离子符号表示)。
(3)写出均由A、B、C、E四种元素组成的二种化合物相互反应的离子方程式