苯甲酸甲酯是一种重要的工业原料,某化学小组采用如下图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯。有关物质的物理性质见下表所示: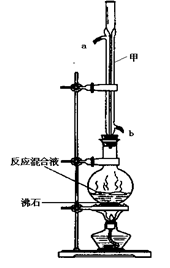
| |
苯甲酸 |
甲醇 |
苯甲酸甲酯 |
| 熔点/℃ |
122.4 |
-97 |
-12.3 |
| 沸点/℃ |
249 |
64.3 |
199.6 |
| 密度/g.cm-3 |
1.2659 |
0.792 |
1.0888 |
| 水溶性 |
微溶 |
互溶 |
不溶 |
Ⅰ.合成苯甲酸甲酯粗产品在圆底烧瓶中加入0.1mol苯甲酸和0.4mol 甲醇,再小心加入 3mL浓硫酸,混匀后,投入几粒沸石,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)甲装置的作用是: ;冷却水从 (填“a”或“b”)口进入。
(2)化学小组在实验中用过量的反应物甲醇,其理由是 。
Ⅱ.粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制
(1)试剂1可以是 (填编号),作用是 。
A.稀硫酸 B.碳酸钠溶液 C. 乙醇
(2)操作2中,收集产品时,控制的温度应在 ℃左右。
(3)实验制得的苯甲酸甲酯精品质量为10g,则苯甲酸的转化率为 (结果保留三位有效数字)。
(4)本实验制得的苯甲酸甲酯的产量低于理论产量,可能的原因是 (填编号)。
A.蒸馏时从100℃开始收集产品 B.甲醇用量多了 C.制备粗品时苯甲酸被蒸出
Ⅰ.配制480 mL 0.5 mol·L-1的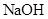 溶液,试回答下列问题:
溶液,试回答下列问题:
(1)选择仪器:完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、________、________等。
(2)计算、称量:需称量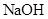 固体的质量为_________________。
固体的质量为_________________。
(3)溶解、冷却,该步实验中需要使用玻璃棒,作用是___________________。
(4)转移、洗涤。洗涤烧杯2~3次是为了______________________________。
(5)定容、摇匀。定容的具体操作是___________________________________。
(6)不规范的实验操作会导致实验结果的误差,下列使所配溶液的物质的量浓度偏高的是 ,偏低的是 (填字母序号)
A.容量瓶洗净后未烘干;
B.在溶解过程中有少量液体溅出烧杯外
C.定容时俯视刻度线;
D.将称量好的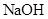 固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
E.定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线
Ⅱ.有同学采用酸性条件下用高锰酸钾标准溶液滴定的方法测定某药品中铁元素的含量,反应原理为 。准确称量该药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.020 0mol/L的
。准确称量该药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.020 0mol/L的 溶液滴定,用去
溶液滴定,用去 溶液12.00 mL.
溶液12.00 mL.
(7)该实验中的试剂2可以是 _________(填编号)。
A.蒸馏水 B.浓盐酸 C.稀硫酸 D.稀硝酸
(8)本实验滴定过程中操作滴定管的图示正确的是_________(填编号)。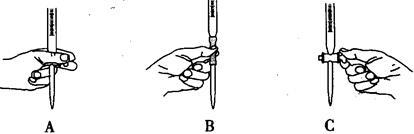
(9)请通过计算,说明该药品含“铁”的百分含量为_________
(用如下装置可以完成一系列实验(图中夹持装置已略去)。
请回答下列问题:
Ⅰ.若在装置A中选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中所设计实验,请填写表中空白:
| B中棉花的位置 |
① |
② |
③ |
④ |
| 所蘸试剂 |
石蕊试液 |
品红溶液 |
淀粉和碘 水混合液 |
氢硫酸 |
| 现象 |
a__________ |
b__________ |
褪色 |
浅黄色 |
| 体现SO2的性质 |
c__________ |
d__________ |
e__________ |
f__________ |
Ⅱ.若在装置A中选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液。回答下列问题:
(1)P中所盛试剂为__________________。
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式__________________;①处包有的某固体物质可能是_____________。
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在整个实验过程中,在③处能观察到的现象为__________________。
(4)反应较长时间后,②处棕黄色褪去,生成无色的IO3-,写出该反应的离子方程式:_______________。
(5)Ⅰ. Ⅱ两实验中尾气均可采用_________溶液吸收。(填化学式)
Ⅰ.实验室常见的几种气体发生装置如图A、B、C所示:
(1)实验室可以用B或C装置制取氨气,如果用B装置制取氨气其化学反应方程式为______________。
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是________(填序号,下同)。
①密度②颜色③溶解性④热稳定性⑤与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可以是下列气体中的__________。
①CO2②NO③Cl2④H2⑤HCl
其中在D装置中连接小烧杯的目的是____________________。
Ⅱ.某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验。
(1)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3,钴的化合价为____________,试写出X的化学式_______________________。
(2)氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。
氨的测定装置(已省略加热和夹持装置)
①装置中安全管的作用原理是_______________________。
②样品中氨的质量分数表达式为_____________________。
三氯化硼(BCl3)是一种重要的化工原料,可用于制取乙硼烷(B2H6),也可做有机合成的催化剂。某兴趣小组拟选用下列装置制备BCl3。
已知:①BCl3的沸点为12.5℃,熔点为-107.3℃;②2B+6HCl 2BCl3↑+3H2↑③硼与铝的性质相似,也能与氢氧化钠溶液反应
2BCl3↑+3H2↑③硼与铝的性质相似,也能与氢氧化钠溶液反应
请回答下列问题:
(1)装置A中发生反应的离子方程式为 。
(2)按气流方向连接各装置的连接顺序为A→ →F(装置可重复使用),实验时应先点燃 处酒精灯(填“A” 或“B”)。
(3)装置E的两个作用是 、 。实验中若不用装置C,可能产生的危险是 。
(4)装置D的作用是 。
(5)BCl3遇水产生大量的白雾,同时生成硼酸(H3BO3),其反应的化学方程式为__________。
(6)设计实验方案验证所得的产品中是否含有硼粉: 。
某化学实验小组利用图所有仪器连接而成制备氮化镁,并探究其实验式。
(1)装置A中反应的化学方程式为__________________________。
(2)按气流方向的连接顺序是(填入仪器接口字母编号):a→()()→()()→()( ) →( ) ( ) →j。
(3)装置E的作用是___________________。
(4)能否将C与D的位置对调并说明理由________________________。
(5)反应过程中,装置F中的末端导管必须始终插入水中,目的是______________________。
(6)请用化学方法确定是否有氮化镁生成,写出实验操作及现象_____________________。
(7)数据记录如下:
| 空硬质玻璃管质量 |
硬质玻璃管与镁的质量 |
硬质玻璃管与产物的质量 |
| 142.312g |
142.480g |
142.550g |
①计算得到实验式MgxN2,其中x=_________________;
②若没有装置D,请比较x与3的大小,并给出判断依据__________________。