标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6gH2S气体④0.2mol氨
气。下列对这四种气体的关系从小到大顺序排列(用序号表示)
| A.体积______________________________ | B.密度__________________________ |
| C.质量______________________________ | D.氢原子数______________________ |
现有下列十种物质:①H2②铝③CaO④CO2⑤H2SO4⑥Ba(OH)2⑦红褐色的氢氧化铁液体⑧氨水⑨稀硝酸⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 |
金属单质 |
氧化物 |
溶液 |
胶体 |
电解质 |
| 属于该类的物质 |
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为__________________________________________________________。
(3)⑩在水中的电离方程式为_______________________________________________。
(4)少量的④通入⑥的溶液中反应的离子方程式为_______________________________。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3=Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是____________(填化学式),氧化剂与还原剂的物质的量之比是___________,当有5.4g Al发生反应时,转移电子的物质的量为____________。该反应的离子方程式为_____________________________
(1)如图是甲烷燃料电池原理示意图,回答下列问题: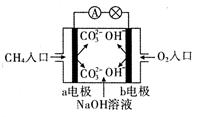
①电池的负极是(填“a”或“b” )极,该极的电极反应式是。
② 电池工作一段时间后电解质溶液的pH(填“增大”、“减小”或“不变”)。
(2)利用甲烷燃料电池及下图所示的装置完成电解饱和食盐水的实验,要求测定产生的氢气的体积,并检验氯气的氧化性。
①设计上述实验装置时,各接口的正确连接顺序为:接、接 A 、 B 接、接。
②实验中,在盛有 KI 淀粉溶液的容器中发生反应的离子方程式为。
③已知饱和食盐水50mL,某时刻测得 H2体积为56mL (标准状况),此时溶液 pH 约为
醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐。
(1)醋酸钠溶液中各离子浓度由大到小的顺序为。
(2)对于醋酸溶液和醋酸钠溶液的下列说法正确的是(填字母,下同)。
| A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小 |
| B.升高温度可以促进醋酸电离,而升高温度会抑制醋酸钠水解 |
| C.醋酸和醋酸钠的混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离 |
| D.醋酸和醋酸钠的混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离 |
(3)物质的量浓度均为 0.1 mol/L 的 CH3COONa 溶液和 CH3COOH 溶液等体积混合(混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是。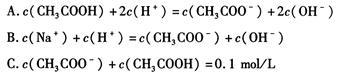
工业上制备 BaC12 的工艺流程图如图所示:
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得: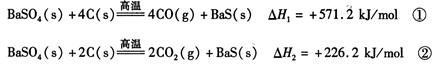
(1)反应C(s) + CO2(g) 2CO(g)的△H =kJ/mol
2CO(g)的△H =kJ/mol
(2)过滤过程中需要使用玻璃棒,玻璃棒的作用是。
(3)盐酸溶解焙烧的固体后,产生的气体用过量 NaOH 溶液吸收,得到硫化钠溶液。 Na2S 水解的离子方程式为。
(4)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,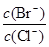 =。[已知:
=。[已知:
Ksp(AgBr) = 5.4×10─13 , Ksp(AgCl) = 2.0×10─10]
工业上制备H2的一种重要方法是: CO(g) + H2O(g)  CO2 (g) + H2(g)△H=Q kJ/mol 。已知该反应的平衡常数K与温度T的关系如图所示。若在一固定的密闭容器中, 850℃ 时发生上述反应,测得容器内各物质的浓度 (mol/L)随时间的变化关系如下表:
CO2 (g) + H2(g)△H=Q kJ/mol 。已知该反应的平衡常数K与温度T的关系如图所示。若在一固定的密闭容器中, 850℃ 时发生上述反应,测得容器内各物质的浓度 (mol/L)随时间的变化关系如下表: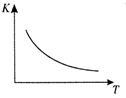
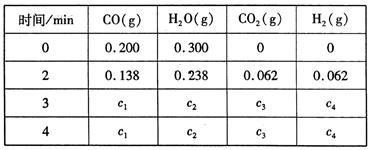
已知:850℃ 时该反应的化学平衡常数K ="1.0" ,请回答下列问题:
(1)Q 0(填“ > ”、“ = ”或“<” )。
(2)可以判断该反应达到化学平衡状态的叙述是(填字母)。
| A.单位时间内减少 CO(g)的浓度等于生成 CO2 (g)的浓度 |
| B.反应容器内的压强不发生变化 |
| C.混合气体中 H2 (g)的浓度不再发生改变 |
| D.氢气的生成速率等于水的生成速率 |
(3)若在850 ℃时向反应容器中充人H2O(g) , K 值(填“增大”、“减小”或“不变”)。
(4)上表中 c2为mol/L , CO(g)的转化率为