(8分)为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
实验二:取上述实验后锥形瓶中清液,进行如下实验:
(1)该清液滴在有色布条上有极强的漂白作用。
(2)该清液中滴加碳酸钠溶液产生白色沉淀。
(3)该清液中滴加稀盐酸可产生大量气体。
(4)该清液加热后变浑浊并产生大量气体。
实验三:该学生设想用下列装置收集实验二中产生的气体作进一步检验。
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有 (写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有 离子;清液加热后产生浑浊的原因是因为生成了 (用化学式表示)。
(2)实验三中,洗气装置内的洗涤液一般用 溶液。
(3)在反应物的量相同情况下,该学生尝试用集气装置A和集气装置B分别和洗气装置相连来收集气体。选用集气装置 (选填“A”或“B”)可收集到更多的气体。经试验,该学生最终选用集气装置B进行下一步实验。其选择装置B的原因是
(4)该学生通过上述实验,写出了氯水和碳酸钙反应的化学方程式为
某学习小组按右图在实验室制取氨气并探究铜的有关性质(部分夹持仪器未画出)。
请回答:
(1)制取氨气的化学方程式是。
(2)① 实验现象为:黑色CuO变为红色(生成单质a);白色无水CuSO4粉末变为蓝色; 同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式。 ②碱石灰的作用是。
(3)将上述生成的单质a在热水浴中进行4个实验,部分实验报告如下表所示。
| 序号 |
实验操作 |
实验现象 |
| Ⅰ |
稀硫酸中加入该单质a |
无明显变化 |
| Ⅱ |
硝酸钠溶液中加入该单质a |
无明显变化 |
| Ⅲ |
硫酸钠溶液中加入该单质a |
无明显变化 |
| Ⅳ |
稀硫酸中加入硝酸钠溶液 |
无明显变化 |
| 再加入该单质a |
有无色气泡;溶液变蓝 |
①实验I、II、III的目的是。
②实验Ⅳ中反应的本质是(用离子方程式表示)。
③将该单质a加入到混有硫酸的过氧化氢溶液中,溶液逐渐变成蓝色,该反应的离子方程式是。
用2.4 mol/L的H2SO4溶液配制100mL浓度为0.2 mol/L的稀H2SO4,回答下列问题:
(1)需用量筒量取2.4 mol/L的H2SO4溶液的体积是mL。
(2)溶液配制的所需的基本步骤如下:
将上述实验步骤A到F按实验过程先后次序排列___________________。
(3)上述实验步骤A、B、E、F都用到的仪器名称为__________。
(4)取上述所配溶液10mL与足量BaCl2溶液反应,生成白色沉淀0.48 g。则该溶液
浓度0.2 mol/L(填“大于”“等于”或“小于”),造成此误差的操作可能
是。
a. 定容时俯视容量瓶; b. 用量筒取2.4 mol/LH2SO4溶液时俯视读数;
c. 容量瓶使用前未干燥;d. 使用的烧杯和玻璃棒未洗涤彻底;
e. 定容时将蒸馏水洒在容量瓶外面
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请回答下列问题:
(1)实验室制取氯气的反应原理为:MnO2+4HCl(浓)  MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
①该反应中被还原的元素是,还原剂是。
②取一定量的浓盐酸使其与二氧化锰反应,产生的氯气在标准状况下的体积为33.6 L,则被氧化的HCl的物质的量为,反应中转移电子数为。
(2)某同学用下列装置制备并检验Cl2的性质。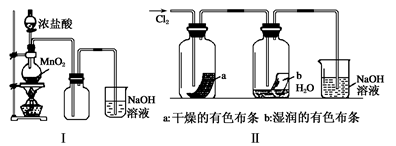

下列说法正确的是
a.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
b.Ⅱ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
c.Ⅲ图中:生成蓝色的烟
(3)若氯气罐发生泄漏,当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是。
a.NaOH b.NaCl c. KOH d. Na2CO3
(4)将SO2和Cl2分别通入装有品红溶液的两个试管中,两溶液的红色均褪去。加热后,有一支试管中的溶液又呈现红色,该试管通入的气体是。
将SO2和Cl2按1:1体积比(同温同压)混合后通入品红溶液中,溶液不褪色。为检验两种气体在溶液中是否发生了氧化还原反应,应向所得溶液加入的试剂是(填化学式)。经实验证明,SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是。
某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是。
| 第1组 |
第2组 |
第3组 |
| S(单质) |
SO2、X、Na2SO3、NaHSO3 |
SO3、H2SO4、Na2SO4、NaHSO4 |
(2)利用下图所示的装置研究SO2的性质:
(熔点:SO2-76.1℃,SO3 16.8℃;沸点:SO2-10℃,SO345℃)
①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是;装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时pH降低,则该反应的离子方程式是。
③乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有40 mL 2.5mol/L NaOH溶液,反应后增重4.8 g,则装置Ⅳ中发生反应的化学方程式是。
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
| 实验方案 |
实验现象 |
| ①用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 |
(A)浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
| ②向新制的H2S饱和溶液中滴加新制的氯水 |
(B)产生气体,可在空气中燃烧,溶液变成浅红色 |
| ③钠与滴有酚酞试液的冷水反应 |
(C)反应不十分强烈,产生的气体可以在空气中燃烧 |
| ④镁带与2 mol·L-1的盐酸反应 |
(D)剧烈反应,产生可燃性气体 |
| ⑤铝条与2 mol·L-1的盐酸反应 |
(E)生成白色胶状沉淀,既而沉淀消失 |
| ⑥向AlCl3溶液滴加NaOH溶液至过量 |
(F)生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告
(1)实验目的:探究同周期元素的金属性和非金属性的递变规律。
(2)实验用品:仪器:①②③④ 试管夹 ⑤ 镊子 ⑥ 小刀 ⑦ 玻璃片⑧ 砂纸⑨ 烧杯等;
药品:钠、镁带、铝条、2 mol·L-1的盐酸、新制的氯水、饱和的H2S溶液、AlCl3溶液、NaOH溶液等。
(3)实验内容:(填写与实验方案相对应的实验现象)
①②③④⑤⑥(用A-F表示)
写出③的离子方程式。
(4)实验结论:。