镁及其化合物在生产和生活中有广泛的应用,试回答下列问题:
(1)常用作耐火材料的镁的化合物与盐酸反应的化学方程式为 。
(2)在军事上金属镁可以用于制造信号弹和焰火,其反应原理用化学方程式可以表示为 。
(3)Mg(OH)2是治疗胃酸过多药品的重要成分之一,其反应原理用离子方程式可以表示为 。
(12分)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式。可用离子交换和滴定的方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预防处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量为________mol,并求出FeClx中X值为__________。
(2)现有一含有FeCl2和FeCl3的混合样品,采用上述方法测得n(Fe): n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为____________。在实验室中,FeCl2可用铁粉和__________反应制备,FeCl3可用铁粉和_______反应制备
(3)铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。
①写出制取铁酸钠的化学方程式:。
②铁酸钠之所以有净水作用,除杀菌外,另一个原因是。
A、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图(反应条件和部分产物略去)。试回答:
(1)E的电子式是。
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是。
(3)物质Z常用于对空气进行杀菌、净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是。
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+)。
(I)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,氢氧化锌溶于氨水可以生成Zn(NH3)42+。回答下列问题:
(1)写出锌和氢氧化钠溶液反应的化学方程式。
(2)写出可溶性铝盐与过量氨水反应的离子方程式。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因。
(II)环境专家认为可以用金属镁将水体中的NO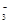 转化为N2,从而清除污染。该反应中涉及的粒子有:H2O、Mg、OH
转化为N2,从而清除污染。该反应中涉及的粒子有:H2O、Mg、OH 、Mg(OH)2、NO
、Mg(OH)2、NO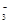 、N2,请将各粒子分别填入以下空格内(不用配平)。
、N2,请将各粒子分别填入以下空格内(不用配平)。
该反应过程中,被氧化与被还原的元素的物质的量之比为。
甲、乙、丙三种物质都含有A元素,只有甲是单质,其转化关系如下: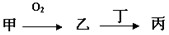
(1)若乙是目前世界倡导需减少排放的温室气体,丁也含有A元素。则含有7个中子的核素A可用符号表示为,丁溶液呈碱性的原因用离子方程式表示为。
(2)若A是非金属元素,其次外层电子是最外层电子数的2倍,则乙在现代通讯中可用于制造,写出一个有丙参加的、能证明碳的非金属性强于A的化学方程式。
(3)若甲是生活中最常用的过渡金属单质,其在点燃条件与氧气反应生成乙。若丁是稀盐酸,则乙→丙的化学方程式为。
(14分)合成氨对化学工业和国防工业具有重要意义。
(1)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
①图A中氨气的体积分数为15%时,H2的转化率为。
②图B中T=450℃,则温度为500℃时对应的曲线是(填“a”或“b”)。
(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为
CH4(g)+H2O(g)  CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
①分析表中数据,判断5 min时反应是否处于平衡状态? (填“是”或“否”),前5 min反应的平均反应速率v(CH4)=。
②该温度下,上述反应的平衡常数K=。
③反应在7~10 min内,CO的物质的量减少的原因可能是(填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度d.充入H2
④若第7分钟时将容器压缩至1L,请在下列坐标系中画出从第7分钟到第11分钟建立新平衡时甲烷浓度随时间的变化曲线。
a