(9分)工业上用软锰矿(主要成分为MnO2)制备高锰酸钾的工艺流程如图所示: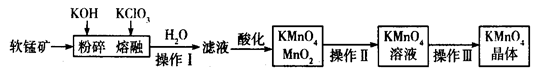
(1)高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强。下列酸能用于酸化高锰酸钾溶液的是____________(填序号)。
| A.盐酸 | B.稀硫酸 | C.硝酸 | D.氢硫酸 |
(2)操作Ⅰ、Ⅱ、Ⅲ的名称分别是______________、_______________、_______________。
(3)软锰矿与过量固体KOH和KClO3在熔融状态下反应时的氧化剂是__________(填化学式)。反应后加水溶解得到的滤液中主要含有KCl和K2MnO4,则滤液酸化时发生反应的离子方程式为______________。
(4)已知KMnO4能与热的经硫酸酸化的Na2C2O4反应生成Mn2+和CO2。取上述制得的KMnO4产品0.33 g,恰好与0.67 g Na2C2O4完全反应,则KMnO4的纯度为___________________%。
现有①氟氯烃 ②二氧化碳 ③二氧化硫 ④废弃塑料制品⑤富含氮、磷元素的污水。请你根据已有的环保知识,选择恰当的序号填空:
(1)能形成酸雨的是;(2)能破坏臭氧层的是;
(3)使水体富营养化的是;(4)导致“白色污染”的是。
蛋白质是构成`生命的基础物质。在鸡蛋、蔬菜、花生油等食物中,富含蛋白质的是。"84消毒液”在日常生活中被广泛使用。该消毒液无色,对某些有色物质具有漂白作用,它的有效成分是(填" KMnO4”或",NaClO")。
实验室制取硝基苯的主要步骤如下:
①配置一定比例的浓硫酸和浓硝酸的混合物,加入反应器
②向室温下的混合液中逐滴加入一定量的苯,充分振荡,混合均匀
③在50-60℃条件下发生反应,直到反应结束
④除去混合酸后,粗产品依次用蒸馏水和5﹪NaOH溶液洗涤,最后用蒸馏水洗涤
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏得到纯硝基苯
填写下列空白:
①配置一定比例的浓硫酸和浓硝酸的混合液时,操作注意事项是
②步骤③中,为了使反应在50-60℃下进行,常用的方法是。
③步骤④中洗涤、分离粗硝基苯使用的仪器是。
④步骤④中粗产品用5﹪NaOH溶液洗涤的目的是。
⑤此反应可表示为。
已知:①有机化学反应因反应条件不同,可生成不同的有机产品。例如: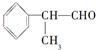
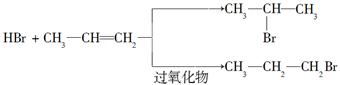
②苯的同系物与卤素单质混合,若在光照条件下,侧链烃基上的氢原子被卤素原子取代;若在催化剂作用下,苯环某些位置上的氢原子被卤素原子取代。
工业上利用上述信息,按下列路线合成结构简式为的物质,该物质是一种香料。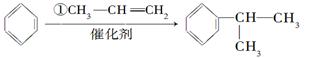
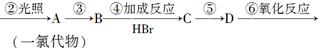
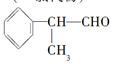
请根据上述路线,回答下列问题:
(1)A的结构简式可能为_____________、____________________。
(2)反应③的反应类型为_________________;反应⑤的条件是_______________
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件,下同):
__________________________________________________。
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取将A直接转化为D的方法,其原因是____________________________。
(5)检验产品中官能团的化学反应方程式为:_____________________________。
(6)这种香料具有多种同分异构体,其中某些物质有下列特征:①其水溶液遇FeCl3溶液呈紫色;②苯环上的一溴代物有两种;③分子中没有甲基。写出一种符合上述条件的物质可能的结构简式:。
某烃A的相对分子质量为84。回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)________。
a.C7H12O2b.C6H14c.C6H14Od.C7H14O3
(2)若烃A为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。
①A的结构简式为________________;
②链烃A与Br2的CCl4溶液反应生成B,B与NaOH的醇溶液共热可得到D,D分子中无溴原子。请写出由B制备D的化学方程式:__________________;
③B与足量NaOH水溶液完全反应,生成有机物E,该反应的化学方程式:____________________________;E与乙二醇的关系是_______________。
(3)若核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为3:2:1,则A的名称为________________。(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为