硫代硫酸钠在工业生产中用途非常广泛。工业上生产Na2S2O3•5H2O的反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,实验室可用如下装置(略去部分加持仪器)模拟生成过程。

Ⅰ.【查阅资料】
(1)硫代硫酸钠(Na2S2O3)易溶于水,在中性或碱性环境中稳定,受热、遇酸易分解。
(2)Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
Ⅱ.【制备产品】
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.酸性高锰酸钾溶液 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和Na2CO3溶液
(2)装置D的作用是检验装置C中SO2的吸收效率,则D中试剂是________________,表明SO2吸收效率低的实验现象是D中溶液________________________。
(3)将C中的混合液加热浓缩、_________、_______(填操作名称)、洗涤、烘干,得到产品。
(4)实验中多余的SO2可以用氢氧化钠溶液吸收。已知常温下H2SO3的Ka1=1.3×10-2、Ka2=6.6×10-8),则亚硫酸氢钠溶液中各离子浓度由大到小的顺序为 ;向亚硫酸氢钠溶液中加入一定量的NaOH,使溶液中c(HSO3-)=c(SO32-),则此时溶液呈 (填“酸性”、“碱性”或“中性”)。在pH=4的H2SO3溶液,试计算溶液中= = 。
= 。
Ⅲ.【测定产品纯度】
(5)为检验制得的产品的纯度,该实验小组称取5.0g的产品配制成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL 0.0lmol·L-1 KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去半分钟不变色时到达滴定终点(假设杂质不参与反应)。实验数据如下表:
实验序号 1 2 3
Na2S2O3溶液体积(mL) 19.98 20.02 21.18
则该产品的纯度是____ ,间接碘量法滴定过程中可能造成实验结果偏高的是____ 。
| A.滴定管末用Na2S2O3溶液润洗 |
| B.滴定终点时俯视读数 |
| C.锥形瓶用蒸馏水润洗 |
| D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡 |
正丁醚常用作有机反应的溶剂。实验室制备正丁醚的反应和主要实验装置如下: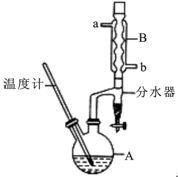
2CH3CH2CH2CH2OH (CH3CH2CH2CH2)2O,反应物和产物的相关数据如下表:
(CH3CH2CH2CH2)2O,反应物和产物的相关数据如下表:
| 相对分子质量 |
沸点/℃ |
密度/(g/cm3) |
水中的溶解性 |
|
| 正丁醇 |
74 |
117.2 |
0.8109 |
微溶 |
| 正丁醚 |
130 |
142.0 |
0.7704 |
几乎不溶 |
①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。
③分离提纯:待A中液体冷却后将其缓慢倒入盛有70 mL水的温度分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11 g。请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为:应先加 。
(2)加热A前,需先从 (填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振摇后静置,粗产物应 (填“上”或“下”)口倒出。
(4)步骤③中最后一次水洗的目的为 。
(5)步骤⑤中,加热蒸馏时应收集 (填选项字母)左右的馏分。
A.100℃ B.117℃ C.135℃ D.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为 ,下层液体的主要成分为 。
(7)本实验中,正丁醚的产率为 (精确到1%)。
(共15分)“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。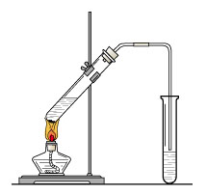
回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式 。
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是 。
(3)浓硫酸的作用是:① ;
② 。
(4)饱和碳酸钠溶液的主要作用是 。
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已省略)。
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为___________________。
(2)装置B中饱和食盐水的作用是_______________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入_______。
| a |
b |
c |
d |
|
| I |
干燥的有色布条 |
干燥的有色布条 |
湿润的有色布条 |
湿润的有色布条 |
| II |
碱石灰 |
硅胶 |
浓硫酸 |
无水氯化钙 |
| III |
湿润的有色布条 |
湿润的有色布条 |
干燥的有色布条 |
干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为______色,说明氯的非金属性大于溴。
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_______。
(6)有人提出,装置F中可改用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式_________,判断改用NaHSO3溶液是否可行______(填“是”或“否”)。
某化学兴趣小组用下图所示装置进行实验,探究硝酸与铁反应的产物。
查阅资料得知:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、﹣3价等氮的化合物。
II.常温时,NO2与N2O4同时存在;在低于0℃时,几乎只有无色的N2O4的晶体存在。
请回答下列问题:
(1)装置中各仪器装入试剂后,接下来由先至后的操作顺序为 。
| A.通入N2 | B.滴入浓HNO3 | C.打开活塞K1 | D.关闭活塞K1 |
(2)装置A中,滴入浓硝酸加热前没有明显现象的原因是 。
(3)反应结束后,打开装置D中的活塞K2,并通入氧气,铁完全溶解于浓硝酸后生成的NO2气体中含有NO的现象为 。
装置D中发生的反应的化学方程式为 。
(4)C装置的作用是 。
(5)反应停止后,装置A中无固体剩余。证明装置A的溶液中是否含有Fe2+,选择的药品是 (填序号)。
a.铁粉b.氯水c.KMnO4溶液d.硫氰化钾溶液
(6)检验是否生成﹣3价氮的化合物,应进行的实验操作、现象及结论是 。
NOx是汽车尾气中的主要污染物之一。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式: 。
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
①写出该反应的热化学方程式: 。
②随温度升高,该反应化学平衡常数的变化趋势是_ 。
(3)在汽车尾气系统中装置催化转化器,可有效降低NOX的排放。
①当尾气中空气不足时,NOX在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式: 。
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOX生成盐。其吸收能力顺序如下:12MgO <20CaO <38SrO<56BaO。原因是 ,元素的金属性逐渐增强,金属氧化物对NOX的吸收能力逐渐增强。
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
①Pt电极上发生的是 反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式: 。