下列说法正确的是 ( )
| A.不用其它试剂便无法区别NaCl、Na2CO3、NaHSO4、AlCl3四种溶液 |
| B.纤维素水解与淀粉水解得到的最终产物不同 |
| C.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量相等 |
| D.用渗析的方法精制氢氧化铁胶体 |
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中的总反应方程式是:
Ni(OH)2 + M =" NiOOH" + MH
已知:6NiOOH + NH3 + H2O + OH-="6" Ni(OH)2 + NO2-
下列说法正确的是
| A.NiMH 电池放电过程中,正极的电极反应式为:NiOOH + H2O + e-= Ni(OH)2 + OH- |
| B.充电过程中OH-离子从阳极向阴极迁移 |
| C.充电过程中阴极的电极反应式:H2O + M + e-=" MH" + OH-,H2O中的H被M还原 |
| D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液 |
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。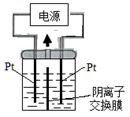
已知:3I2+6OH—=IO3—+5I—+3H2O
下列说法不正确的是
| A.右侧发生的电极方程式:2H2O+2e—=H2↑+2OH— |
| B.电解结束时,右侧溶液中含有IO3— |
| C.电解槽内发生反应的总化学方程式KI+3H2O=KIO3+3H2↑ |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变 |
将下图所示实验装置的 K 闭合,下列判断正确的是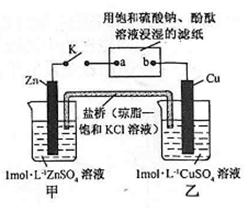
| A.Cu 电极上发生还原反应 |
| B.电子沿 Zn→a→b→Cu 路径流动 |
| C.片刻后甲池中c(SO42-)增大 |
| D.片刻后可观察到滤纸b点变红色 |
某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl— Cl2↑+H2↑ Cl2↑+H2↑ |
| B.断开K2,闭合K1时,石墨电极附近溶液变红 |
| C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl— |
| D.断开K1,闭合K2时,石墨电极作正极 |
用石墨电极电解CuCl2溶液(见右图)。下列分析正确的是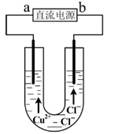
| A.a端是直流电源的负极 |
| B.通电使CuCl2发生电离 |
| C.阳极上发生的反应:Cu2++2e-=Cu |
| D.通电一段时间后,在阴极附近观察到黄绿色气体 |