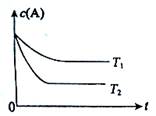
(2013)反应A(g)  B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。
回答下列问题:
(1)上述反应的温度T1 T2,平衡常数K(T1) K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为 。
②反应的平衡常数K= 。
③反应在0~5min区间的平均反应速率v(A)= 。
卤代烃在碱性醇溶液中能发生消去反应。例如:
下图是八种有机化合物的转换关系。
请回答下列问题:
(1)上述框图中,属于消去反应的是(填序号).
(2)①是______________(填反应类型),
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式:
___________________________________________________。
(4)C2的结构简式是__________________。
F1的结构简式是________________。
F1和F2互为________________。
(5)上述八种化合物中,属于二烯烃的是________。
二烯烃的通式是________。
已知某烃类化合物A的相对分子质量为84:
(1)若分子中含有一个碳碳双键,且分子中只有一种类型的氢原子
A的结构简式为
A中的碳原子是否都处于同一平面?(填“是”或者“不是”)。
(2)若分子中无碳碳双键,且分子中只有一种类型的氢原子
A的结构简式为
其名称为
请根据官能团的不同对下列有机物进行分类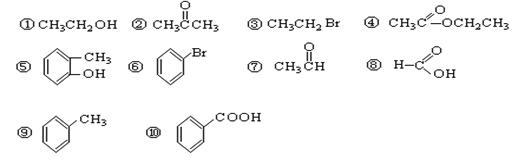
(1)芳香烃: ;(2)卤代烃:;
(3)醇: ;(4)酚: ;(5)醛: ;
(6)酮: ;(7)羧酸: ;(8)酯:。
(Ⅱ)
⑴键线式 表示的分子式。
表示的分子式。
⑵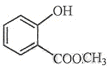 中含有的官能团的名称为。
中含有的官能团的名称为。
⑶书写该物质的名称: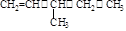
今有分子量为58的几种有机物,试推断符合条件的有机物的分子式或结构简式
(1)若该有机物为烃,则分子式为,其中带有支链的同分异构体在核磁共振氢谱图中有个吸收峰
(2)若该有机物是一种饱和一元脂肪醛,则其与新制氢氧化铜悬浊液在加热条件下反应的化学方程式为。
(3)若该有机物1mol能与足量银氨溶液作用可析出4molAg,则其结构简式为。
(4)若该有机物能与金属钠反应,又能使溴的四氯化碳溶液褪色,则其结构简式为,(注羟基连在双键上的有机物极不稳定)该物质生成高分子化合物的化学方程式为。
选用适当的试剂和方法除去下列物质中的杂质(括号内)填下表:
除杂质的试剂:①氢氧化钠溶液②溴水③生石灰④饱和碳酸钠溶液
除杂质的方法:A分液 B萃取 C蒸馏 D过滤
| 混合物 |
除杂质的试剂 |
除杂质的方法 |
| 苯(苯酚) |
(1) |
(4) |
| 酒精(水) |
(2) |
(5) |
| 乙酸乙酯(乙酸) |
(3) |
(6) |