反应A(s)+2B(g)  2C(g)在密闭容器中达到平衡。
2C(g)在密闭容器中达到平衡。
(1)若升高温度能使C的物质的量减少,则正反应是________热反应;
(2)若增加A的物质的量,平衡________移动;
(3)若增大压强,则平衡________移动;
(4)若增加C的浓度,则B(g)的转化率________(填“增大”“减小”或“不变”)。
碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。
(1)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
I.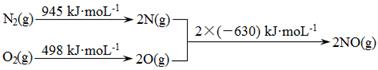
II.N2(g)+ O2(g)  2NO(g)ΔH1
2NO(g)ΔH1
2CO(g) + O2(g) 2CO2 (g) ΔH2=" -565" kJ·mol-1
2CO2 (g) ΔH2=" -565" kJ·mol-1
①ΔH1=。
②在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式。
(2)电化学气敏传感器法测定汽车尾气。其中CO传感器的工作原理如图所示,则工作电极的反应式为
(3)工业上可以用NaOH溶液或氨水吸收过量的SO2,分别生成NaHSO3、NH4HSO3,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中c(SO32-)较小的是,用文字和化学用语解释原因。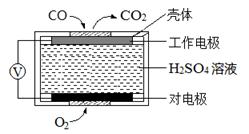
(4)T℃时,在 2L恒容密闭容器中,加入Fe3O4、CO各1.0 mol ,10 min反应达到平衡时,容器中CO2的浓度是0.4 mol /L。
①能证明该反应达到化学平衡的是(选填字母)。
a.容器内压强不再变化 b.容器内CO、CO2物质的量比为1 : 1
c.容器内气体的质量不再变化 d.生成CO2的速率与消耗CO的速率相等
②l0 min内,反应的平均反应速率v (CO2)=。
③T℃时,该反应的平衡常数K=。
Al2O3、Al(OH)3都是重要化工原料。根据要求回答问题:
Ⅰ、电解法制高品质Al(OH)3装置如下(中间用离子交换膜隔开):
4Na[Al(OH)4]+2H2O 4Al(OH)3↓+4NaOH+O2↑+2H2↑
4Al(OH)3↓+4NaOH+O2↑+2H2↑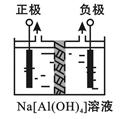
(1)产物Al(OH)3在区(填“阴极”或“阳极”)沉积;
(2)电解中转移2mol e—时,将制得__________mol的Al(OH)3。
Ⅱ、制取纳米Al2O3需要纯净的硫酸铝。现有0.05mol·L-1硫酸铝溶液,经检测,含有Fe2+、Fe3+。可按下述操作提纯:往溶液中加足量H2O2充分反应,再用试剂X调节溶液pH=3.5。(室温下,0.1mol·L-1的Fe2+、Al3+开始沉淀的pH分别为7.0和3.7,Fe3+完全沉淀的pH=3.2)
(3)纳米氧化铝分散在分散剂中将形成胶体。则纳米氧化铝的直径约为m。
(4)检验硫酸铝溶液含有Fe3+时,所采用的试剂及现象是。
(5)往溶液中加入H2O2的作用是(用离子方程式表示)。
(6)加入的X试剂(填选项编号)是。
| A.CuO | B.Al(OH)3 | C.NaOH | D.NaHCO3 |
若调节后溶液的pH偏离3.5,可能带来的后果是。
选做【化学——有机化学基础】(12分)枯茗醛可用作食用香精。现由枯茗醛合成兔耳草醛,其合成路线如下:
已知醛在一定条件下发生如下反应:
请回答下列问题:
(1)写出试剂X的结构简式:____________。
(2)写出有机物B中所含官能团的名称为_____________;A→B的反应类型为__________。
(3)检验B中的官能团所需的试剂是_________(填序号)。
| A.银氨溶液 稀盐酸 溴水 |
| B.新制氢氧化铜悬浊液稀硫酸酸性高锰酸钾溶液 |
| C.新制氢氧化铜悬浊液 稀盐酸 溴水 |
| D.银氨溶液稀硫酸酸性高锰酸钾溶液 |
(4)写出有机物C生成兔耳草醛的化学方程式:_________________________。
(5)芳香族化合物Y与枯茗醛互为同分异构体,Y具有如下特征:
a.不能发生银镜反应,可发生消去反应;
b.核磁共振氢谱显示:Y消去反应产物的苯环上只存在一种化学环境的氢原子;
写出Y可能的结构简式:_____________、______________。
选做【化学——物质结构与性质】(12分)
(1)X难溶于水、易溶于有机溶剂,其晶体类型为___________;Cu2+的核外电子排布式为__________。
(2)M中所含元素的电负性由大到小顺序为_______,N原子以___________轨道与O原子形成 键。
键。
(3)上述反应中断裂和生成的化学键有___________(填序号)。
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
(4)铜晶胞的结构如图所示,铜晶体中每个铜原子周围距离最近的铜原子数目为________。
(18分)化学反应原理在生产和科研中有着重要的应用,请利用相关知识回答下列问题。
(1)一定条件下在密闭容器中加入NH4I发生反应:
则反应a的平衡常数表达式为_________;达到平衡后,扩大容器体积,反应b的移动方向_______(填正向、逆向或不移动)
(2)氮元素的+4价氧化物有两种,它们之间发生反应:2NO2 N2O4∆H < 0,将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4∆H < 0,将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
| A.b点的操作是压缩注射器 |
B.c点与a点相比, 增大, 增大, 减小 减小 |
| C.若不忽略体系温度变化,且没有能量损失,则b、c两点的平衡常数Kb>Kc |
D.d点: (正)> (正)>  (逆) (逆) |
(3)利用反应 构成原电池,能消除氮氧化物的排放,减轻环境污染,装置如图所示。
构成原电池,能消除氮氧化物的排放,减轻环境污染,装置如图所示。
①电极a为__________极,其电极反应式为_________________。
②当有2.24LNO2(标准状况下)被处理时,转移电子为____________mol。
③为使电池持续放电,该离子交换膜需选用____________交换膜。
(4)使用硼氢化钠(NaBH4)为诱导剂,可使Co2+与肼(N2H4)在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式_______________________。
②在纳米钴的催化作用下,肼(N2H4)可分解生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示,为抑制肼的分解,可采取的合理措施有____________(任写一种)。