向84消毒液(含氯化钠和次氯酸钠)中加入足量浓盐酸,分步反应为 、 。
简要回答下列问题
(1)以淀粉为原料生产葡萄糖的水解过程中,可用什么方法来检验淀粉的水解是否完全?
_______________________________________________________。
(2)成熟苹果的汁液能与银氨溶液发生反应,试解释原因。
_______________________________________________________。
(3)如何鉴别蚕丝和人造丝(纤维素)织物?
_______________________________________________________。
(4)乙醇和乙酸的官能团的名称分别是什么?
_______________________________________________________。
城市居民使用的管道气体燃料中,有天然气(主要成分是 )和“煤气”(主要成分是
)和“煤气”(主要成分是 和
和 )。它们燃烧反应的化学方程式如下:
)。它们燃烧反应的化学方程式如下:
试判断:
(1)燃烧相同体积的管道煤气和天然气,消耗氧气体积较大的是哪种?____________。
(2)适用于管道煤气的灶具在改为用于天然气时,需将进风口改大还是改小?如不改造进风口,可能产生什么不良后果?_____________________________________。
(3)管道煤气中除 和
和 外,还含少量甲烷、乙烷、丙烷、丁烷(沸点:-0.5℃)等气态烃,请解释为什么在严寒的冬季,管道煤气有时会出现火焰变小或断续现象。
外,还含少量甲烷、乙烷、丙烷、丁烷(沸点:-0.5℃)等气态烃,请解释为什么在严寒的冬季,管道煤气有时会出现火焰变小或断续现象。
___________________________________________________________。
书写化学方程式,并注明反应类型
(1)甲烷和氯气反应生成一氯甲烷_______________________________________。
(2)乙烯和溴水反应_______________________________________。
(3)苯和液溴在溴化铁催化下反应_______________________________________。
(4)由丙烯(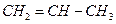 )合成聚丙烯_______________________________________。
)合成聚丙烯_______________________________________。
(5)乙醇和乙酸在浓 催化并加热条件下反应________________________。
催化并加热条件下反应________________________。
下列物质中,互为同位素的是(填序号,下同),互为同素异形体的是,互为同系物的是,互为同分异构体的是。
①金刚石; ②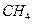 ; ③
; ③ ; ④
; ④ ;⑤
;⑤
⑥石墨; ⑦ ; ⑧
; ⑧
已知烃B分子内C、H原子个数比为1︰2,相对分子质量为28;有如下的转化关系: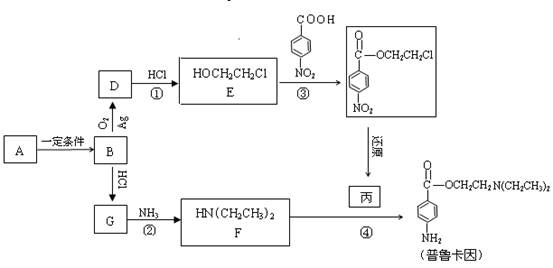 回答
回答
(1)A可能属于下列哪类物质___________。
a.醇 b.卤代烃 c.酚 d.羧酸
(2)反应②可表示为:G + NH3 → F + HCl (未配平),该反应配平后的化学方程式是
。
(3)③的反应类型是_________________。
(4)普鲁卡因有两种水解产物丁和戊。
①戊与互为同分异构体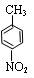 ,戊的结构简式是_____________________。
,戊的结构简式是_____________________。
②D的红外光谱表明分子内除C—H键、C—C键外还含有两个C—O单键,且是环状化合物,写出D与F在一定条件下反应生成丁的化学方程式是
。