(16分)某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
请回答:
(1)写出步骤Ⅰ反应的离子方程式: ; 。
(2)试剂X是 。由溶液D是 。
(3)在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。
一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)溶液E中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因 。
(5)用固体F继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;写出反应的化学方程式 ,
(6)工业上常用溶液E经进一步处理可制得净水剂Na2FeO4,流程如下:
①测得溶液E中c(Fe2+) 为0.2 mol·L-1,若要处理1 m3溶液E,理论上需要消耗25 % 的H2O2溶液___kg。
②写出由Fe(OH)3制取Na2FeO4的离子方程式___________。
化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
Ⅰ.一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应2HI H2+I2,H2物质的量随时间的变化如图所示。0~2 min内 的平均反应速率v(HI)=_________。该温度下,H2(g)+I2(g)
H2+I2,H2物质的量随时间的变化如图所示。0~2 min内 的平均反应速率v(HI)=_________。该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=_____。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则_____是原来的2倍。
2HI(g)的平衡常数K=_____。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则_____是原来的2倍。
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
Ⅱ.常温下,将pH=3的盐酸a L分别与下列三种溶液混合,
结果溶液均呈中性。
①浓度为1.0 ×l0-3 mol.L-1的氨水b L;
②c(OH-)=1.0×10-3mol.L-l的氨水c L;
③c(OH-)=1.0×10-3 mol ·L-1的氢氧化钡溶液d L。则a、b、c、d之间由大到小的关系是:。
Ⅲ.工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人体及生态系统产生很大的伤害,必须进行处理。还原沉淀法是常用的一种方法。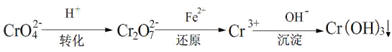
(1)转化过程中存在平衡2CrO42- + 2H+ Cr2O72- + H2O能说明反应到达平衡状态的是。
Cr2O72- + H2O能说明反应到达平衡状态的是。
| A.CrO42-和Cr2O72-的浓度相同 | B.2ν(Cr2O72-)=ν(CrO42-) |
| C.溶液的pH值保持不变 | D.溶液颜色保持不变 |
(2)若1L转化后所得溶液中含铬元素质量为28.6g,CrO42-有10/11转化为Cr2O72-(已知铬元素相对原子质量为52)。
①转化后所得溶液中c(Cr2O72-)=。
②已知:常温下该反应的平衡常数K=1014,上述转化后所得溶液的pH为。
(3)若常温下Ksp(Cr(OH)3) =10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至。
金属元素及其化合物在科学研究和生产生活中有着广泛的用途。
(1)氢气还原氧化铜时,产生的红色物质,冷却后加入稀硫酸发现溶液呈淡蓝色,写出该现象发生的离子方程式 。
(2)铝的某种超原子结构(Al13)具有40个价电子时最稳定。请预测稳定的Al13所带的电荷数为。取铝合金(含铝90%)1.5 g与80 mL 3mol•L-1 盐酸充分反应(合金中其它成分不参加反应)。滤去不溶物,将滤液稀释到100mL,取出稀释液5mL,加入0.6 mol•L-1 的氨水使Al3+ 恰好完全沉淀。上述铝合金和盐酸反应的过程中生成氢气_________L(标准状况)。使Al3+ 恰好完全沉淀时,消耗氨水_________mL。
甲烷的电子式是,结构式是,其空间构型是,在光照的条件下,甲烷可以和氯气发生反应。甲烷在空气中完全燃烧的化学方程式。
用“>”或“<”回答下列问题:
(1)气态氢化物的稳定性:H2OH2S
(2)原子半径:MgNa
(3)碱性:NaOHMg(OH)2
分析下列实例,根据已有的知识和经验填写影响反应速率的因素:
(1)夏天食物易变质:。
(2)氯酸钾与二氧化锰混合共热可快速产生氧气:。
(3)粉状的碳酸钙与盐酸反应比块状的碳酸钙反应快:。
(4)硫在氧气中比在空气中燃烧快:。