(14分)下图为细菌冶铜和火法冶锎的主要流程。
(1)硫酸铜溶液一般不呈中性,原因是__ _____(用离子方程式表示)。写出电解硫酸铜溶液的化学方程式:_____ _________(电解过程中,始终无氢气产生)。
(2)细菌冶金又称微生物浸矿,是近代湿法冶金工业上的一种新工艺。细菌冶铜与火法冶铜相比,优点为_____ ___________(写出一点即可)。
(3)用惰性电极分别电解浓的氯化铜溶液和硫酸铜溶液。电解浓的氯化铜溶液时发现阴极有金属铜生成,同时阴极附近会出现棕褐色溶液。而电解硫酸铜溶液时,没有棕褐色溶液生成。
下面是关于棕褐色溶液成分的探究
①有同学认为,阴极附近出现的棕褐色溶液是氯气反应的结果,你认为他的猜测是否正确?______(填“正确”或“不正确"),原因是_____ _ _____。
资料1:一般具有混合价态(指化合物中同一元素存在两种不同的化合价,如Fe3O4中的 Fe元索)的物质的颜色比单一价态的物质的颜色要深。
资料2:CuCl微溶于水,能溶于浓盐酸。
②猜想:棕褐色溶液中可能含有的离子是____ ____(填3种主要离子符号)。
③验证猜想:完成实验方案(配制棕褐色溶液)。
取少量____ ____固体于试管中,加入__ _____使其溶解,再加入___ ____溶液,观察现象。
④已知电解前,U形管中加入了100mL0.5 mol.L-1 CuCl2溶液,电解结束时电路中一共转移了0.03 mol电子,且阴极生成0.64 g铜,则形成的低价阳离子的物质的量为_____mol。
按要求书写下列反应的离子方程式
(1)CuSO4溶液与过量Ba(OH)2溶液反应:
(2)Al2(SO4)3溶液中加入过量氨水:
(3)将过量SO2气体通入冷氨水中:
(4)向NaAlO2溶液中通入过量CO2:
(5)0.01 mol·L-1 NH4Al(SO4)2溶液与0.02 mol·L-1 Ba(OH)2溶液等体积混合:
利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应。常用来生产液氨和氨水。
完成下列填空:
(1)右图表示合成氨时生成1mol生成物时的能量变化,E的单位为kJ。请写出合成氨的热化学方程式 (热量用E1、E2或E3表示)。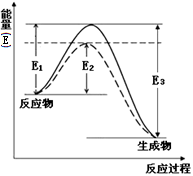
该图中的实线与虚线部分是什么反应条件发生了变化? 。
(2)在一定温度下,若将4amol H2和2amol N2放入VL的定容密闭容器中,2分钟后测得N2的转化率为50%,则该段时间用H2表示的反应速率为 摩尔/(升–秒)。若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是 (填“正向移动”“逆向移动”或“不移动”)。
(3)液氨和水类似,也能电离:2NH3 NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K 2×10-30(填“<”、“>”或“=”);
NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K 2×10-30(填“<”、“>”或“=”);
②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒物质的量大小排列为:
(4)工厂生产的氨水作肥料时需要稀释。用水稀释0.1mol/L稀氨水时,溶液中随着水量的增加而减少的是 。
a.c(NH4+)/c(NH3•H2O)b.c(NH3•H2O)/c(OH-)
c.c(OH-)/c(H+) d.c(H+)/c(NH4+)
硫化钠是一种重要的化工原料。工业上用硫酸钠与碳反应得到硫化钠。反应方程式如下:
Na2SO4 + 2C Na2S + CO2↑
Na2S + CO2↑
完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子有 种能级不同的电子。
(2)下列可以证明二氧化碳是非极性分子的事实是 (填编号)
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)硫化钠在一定条件下会与硫单质反应生成多硫化钠(Na2SX)。在碱性溶液中,Na2SX与NaBrO3反应生成Na2SO4与NaBr。若Na2SX与NaBrO3反应的物质的量之比为3:16,则 x = 。
(4)写出硫氢化钠与少量硫酸铜溶液反应的离子方程式 。能否用硫酸铜溶液来鉴别硫化钠溶液和硫氢化钠溶液?请简述实验操作和现象并说明自己的观点: 。
(5)已知:H2S Ki1 = 9.1×10-8 Ki2 = 1.1×10-12 HF Ki = 3.5×10-4
H2SO3 Ki1 = 1.5×10-2 Ki2 = 1.0×10-7 HAc Ki = 1.75×10-5
若用右图的装置,用硫化钠固体和下列溶液制取硫化氢气体,可选用的试剂是 。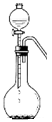
a.硝酸 b.亚硫酸氢钠 c.氢氟酸 d.醋酸
综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:
(1)反应①~⑤中,属于氧化还原反应的是 。
(2)写出反应②的离子方程式 。
(3)X溶液中的主要阳离子是Na+和 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;
③ ;④加适量盐酸;⑤ (请补全缺少的实验步骤)。
(5)检验纯碱样品中是否含NaCl应选用的试剂是 。
海带具有从海水中富集碘的能力,下面是从海带中提取碘单质的流程:
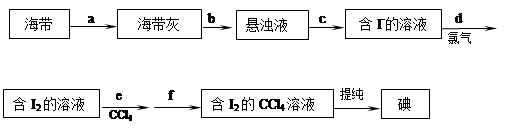
试回答:
(1)步骤a的操作名称是 ,步骤b中所加的物质是 。
(2)步骤c的操作名称是 ;该操作中涉及到的玻璃仪器有漏斗、烧杯和 。
(3)步骤d中发生反应的离子方程式为 。
(4)步骤e的操作名称是 ,操作时在含I2的溶液中加入CCl4,振荡、静置后,液体分为两层,下层液体呈 色。
(5)步骤f的操作名称是分液,所用的主要仪器是 。