甲、乙、丙、丁、X是中学阶段的五种常见物质,它们的转化关系如下图所示(部分产物已略去):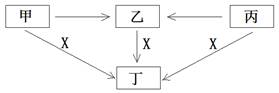
(1)若甲、乙、丙、丁均为化合物,且焰色反应均呈黄色。丙是淡黄色固体,常温下X是一种无色无味气体。则:
①甲和X生成丁的化学方程式为:
②丙和X生成丁的反应中还原剂是 (填化学式),有0.2mol丁生成时,电子转移的数目是 。
(2)若甲、乙、丙、丁都含有地壳中含量最多的金属元素,且丙受热时分解生成乙。X、丁溶液的焰色反应均为紫色(透过蓝色钴玻璃)。
①图中五个转化中属于氧化还原反应的数目是
| A.2 | B.3 | C.4 | D.5 |
②乙和X生成丁的离子方程式为 。
③溶液中生成的丙能够净水,其原因是 。
(12分)阅读以下信息,并回答问题
数十亿年来,地球上的物质不断地变化。大气的成分也发生了很大的变化。下表是原始大气和目前空气的主要成分: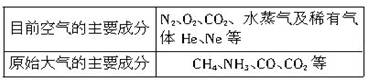
用上表所涉及的分子填写下列空白:
(1)由极性键构成的非极性分子有________和__________(填写化学式)。
(2)极易溶于水、其水溶液呈碱性的物质的分子是_________(填写化学式),它之所以极易溶于水,是因为它的分子和水分子之间可形成_______键。
(3)分子中不含孤对电子的分子(除稀有气体外)为__________(填写化学式),它的立体构型为____________。
(4)CO的结构可表示为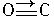 ,与CO结构最相似的分子是________(填写化学式),这两种结构相似的分子中,分子的极性________(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫________键。
,与CO结构最相似的分子是________(填写化学式),这两种结构相似的分子中,分子的极性________(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫________键。
(5)随着原始大气中O2的缓慢增加,CH4、NH3、CO等气体逐渐被氧气氧化而缓慢地减少,使大气的成分逐渐演化成目前空气。原始大气中NH3可转化为目前空气中的__________(填化学式)。下
(6)人工模拟是当前研究的热点。有研究表明,化合物X可用于研究模拟酶,当其结合或Cu(I)(I表示化合价为+1)时,分别形成a和b:下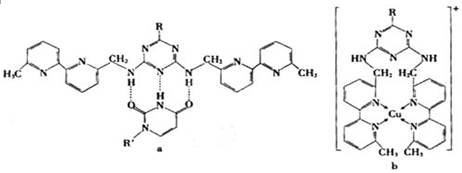
分析a和b中微粒间的相互作用(包括化学键和分子间相互作用),试指出其不同点:
a中含,b中含。(用“氢键”、“配位键”、“极性键”、“非极性键”等填空)
(8分)(1)短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第___族。
|
|
|
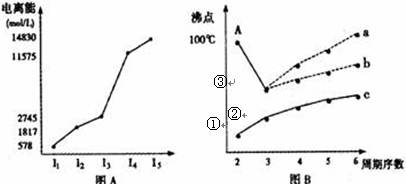


A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2。C、D的电离能数据如下(kJ·mol―1):
| I1 |
I2 |
I3 |
I4 |
|
| C |
738 |
1451 |
7733 |
10540 |
| D |
577 |
1817 |
2745 |
11578 |
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显价,D显价;
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含___个σ键,___个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是______________________________
| 单键 |
双键 |
叁键 |
||
| AB |
键能(kJ·mol―1) |
357.7 |
798.9 |
1071.9 |
| 甲 |
键能(kJ·mol―1) |
154.8 |
418.4 |
941.7 |
(4)E能与AB形成配合物,其中E提供______________,AB提供________________。
(5)下列晶胞中,阳离子与阴离子的个数为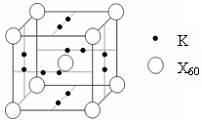
有A、B、C、D、E、F六种前四周期元素,原子序数A<B<C<D<E<F。A原子只有一个电子层且只含1个电子;B、C两元素的基态原子具有相同能级,且I1(B)>I1(C),其中基态B原子的2p轨道上有3个未成对电子;D原子s电子数比p电子数少4;E原子的3p轨道上得到1个电子后不能再容纳外来电子;F为周期表前四周期中电负性最小的元素
(1)写出下列元素的元素符号:下
C___________ F_____________
(2)写出E元素原子的价电子轨道表示式___________________
(3)B、C两元素原子的电负性大小: B_______C(填“<”或“>”)
(4)A2C与A2D的熔沸点:A2C_______A2D (填“<”或“>”)
(5)A、C两元素按原子个数比为1:1结合成的化合物化学式为_____________
(6)BA3的中心原子杂化方式为______杂化,该化合物的空间构型为_____________.
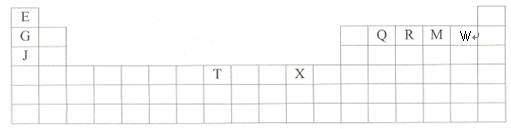
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
|