 已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
| A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
(1)若溶液中只溶解了一种溶质,该溶质是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
(2)若上述关系中D是正确的,混合后溶液中的溶质为 。
(3)25 ℃时,将a mol·L-1的氨水与b mol·L-1盐酸等体积混合,反应后溶液恰好显中性,则混合前a b(填“>”、“<”、或“=”), 用a、b表示NH3·H2O的电离平衡常数为 。
已知下列反应的反应热:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H=-870.3kJ∕mol
②C(S)+O2(g)=CO2(g)△H=-393.5kJ∕mol
③2C(S)+2H2(g)+O2(g)=CH3COOH(l) △H=-488.3kJ∕mol
请写出H2燃烧热的热化学方程式 。
。
写出下列物质的电离方程式(在水溶液中)。
(1)H2SO4;
(2)H2CO3;
(3)NaHSO4;
(4)NaHCO3 ;
;
(5)Cu(OH)2。
下列物质中:(填序号)
A .KCl(s)B.C2H5OH(l) C.
.KCl(s)B.C2H5OH(l) C. Cl2(g)D.冰醋酸 E.BaSO4(s)
Cl2(g)D.冰醋酸 E.BaSO4(s)
F.NaHSO4(s) G.石墨(s)H.蔗糖(s) I.NaOH溶液
(1)能直接导电的是;(2)属于强电解质的是;
(3)属于弱电解质的是;(4)属于非电解质的是 。
。
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):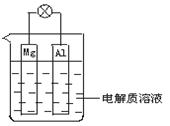
(1)电解质溶液为稀H2SO4时,灯泡____(填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题).
a.若灯泡亮,则Mg电极上发生的反应为:_______________;Al电极上发生的反应为:_______________.
b.若灯泡不亮,其理由为:_________________________________.
(2)电解质溶液为NaOH(aq)时,灯泡____(填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题).
a.若灯泡亮,则Mg电极上发生的反应为:_______________;Al电极上发生的反应为:_______________.
b.若灯泡不亮,其理由为:________________________.
位于短周期的四种主族元素A、B、C、D,原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。E是地壳中含量最高的金属。
根据你的推断完成下列问题:
(1)B元素的名称为________周期表的位置_______E的元素符号为_________。
(2)由A、B两种元素形成的原子个数比为1∶1的化合物的电子式__________。
(3)写出由上述元素形成的具有漂白作用的两种物质的化学式_____________、
____________________。
(4)用电子式表示C与D形成化合物的过程____________________________。
(5)写出E的最高价氧化物与强碱反应的离子方程式_____________________。