Ⅰ.制水煤气的主要化学反应方程式为:C(s)+H2O(g) CO(g)+H2(g),此反应是吸热反应。
CO(g)+H2(g),此反应是吸热反应。
①此反应的化学平衡常数表达式为 ;
②下列能提高碳的平衡转化率的措施是 。
| A.加入C(s) |
| B.加入H2O(g) |
| C.升高温度 |
| D.增大压强 |
E.将碳研成粉末
Ⅱ.研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)已知石墨的标准燃烧热为y kJ·mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量。则石墨与氧气反应生成CO的热化学方程式为:
________________________________________________________________。
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是:
________________________________________________________________。
②由MgO可制成“镁—次氯酸盐”燃料电池,其装置示意图如图1所示,该电池反应的离子方程式为:_____________________________________________________________。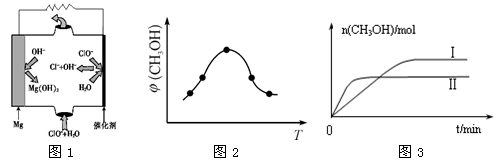
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g)  CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的ΔH__________(填“>” “<”或“=”)0。
②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ 对应的平衡常数大小关系为KⅠ__________________KⅡ(填“>” “<”或“=”)。
③一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
| 容 器 |
甲 |
乙 |
| 反应物投入量 |
1molCO2 3molH2 |
a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为____________________。
分别取一定质量的甲烷、乙炔、苯、己烯、甲苯,完全燃烧后都生成 m mol CO2和n mol H2O。
(1)若m=n,该烃是____________。
(2)若m=2n,该烃是___________。
(3)若2m=n,该烃是___________。
(4)若4m=7n,该烃是__________。
①硝基苯 ②环己烷 ③甲苯 ④溴苯 ⑤邻二甲苯 ⑥三硝基甲苯,其中不能由苯通过一步反应直接制取的是____________。(填编号)
人们对苯的认识有一个不断深化的过程。
(1)1834年德国科学家米希尔里希,通过蒸馏安息香酸(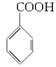 )和石灰的混合物得到的液体被命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式_______________________________________。
)和石灰的混合物得到的液体被命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式_______________________________________。
(2)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出C6H6的一种含三键且无支链链烃的结构简式________________________________。苯不能使溴水褪色,性质类似烷烃,任写一个苯发生取代反应的化学方程式_____________________________________。
烷基取代苯 可以被KMnO4的酸性溶液氧化生成
可以被KMnO4的酸性溶液氧化生成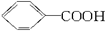 ,但若烷基R中直接与苯环连接的碳原子上没有C—H键,则不容易被氧化得到
,但若烷基R中直接与苯环连接的碳原子上没有C—H键,则不容易被氧化得到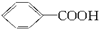 。现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为
。现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为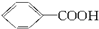 的异构体共有7种,其中的3种是
的异构体共有7种,其中的3种是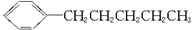 、
、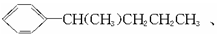
 ,请写出其他的4种结构简式:________________、__________________、________________、________________。
,请写出其他的4种结构简式:________________、__________________、________________、________________。
某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是 。
(2)利用下图所示的装置研究SO2的性质:
(熔点:SO2 -76.1℃,SO3 16.8℃;沸点:SO2 -10℃,SO3 45℃)
①装置I模拟工业生产中SO2催化氧化的反应,其化学方程式是 。
②甲同学按I、II、III、IV的顺序连接装置,装置II的作用是 ;装置III中溶液逐渐褪色,生成Mn2+,同时pH降低,则该反应的离子方程式是 。
③乙同学按I、II、IV的顺序连接装置,若装置IV中有40 mL 2.5mol•L-1 NaOH溶液,反应后增重4.8 g,则装置IV中发生反应的化学方程式是 。