(2014届山东省日照市高三3月模拟考试理综化学试卷)
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。工业设计生产NaClO2的主要流程如下:
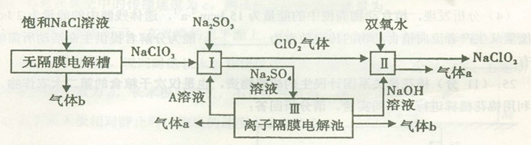
(1)A的化学式是 ,装置III中A在 极区产生。
(2)II中反应的离子方程式是 。
(3)通电电解前,检验III中阴离子的方法和步骤是 。
(4)为防止II中制备的NaClO2被还原成NaCl,应选合适的还原剂,除双氧水外,还可以选择的还原剂是 (填字母编号)。
a.Na2O2 b.FeCl2 c.Na2S
(5)常温时,HClO2的电离平衡常数Ka=1.07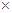 10-2mol·L-1,II中反应所得NaClO2溶液(含少量NaOH)的pH=13,则溶液中
10-2mol·L-1,II中反应所得NaClO2溶液(含少量NaOH)的pH=13,则溶液中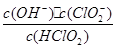 = 。
= 。
(6)气体a、b与氢氧化钠溶液可构成燃料电池,用该电池电解200 mL 0.5 mol·L-1的CuSO4溶液,生成铜3.2 g,此时所得溶液中离子浓度由大到小的顺序是
有 A、B、C三种短周期元素。A-离子的电子层 结构和氖原子相同;短周期元素中B的金属性最强;C的原子核内质子数是B的次外层电子数的2倍。试推断:
结构和氖原子相同;短周期元素中B的金属性最强;C的原子核内质子数是B的次外层电子数的2倍。试推断:
⑴. A元素的名称是______、B在周期表的位置表示为__ ____、C的原子结构示意图为__ ____;
⑵. B的氢氧化物的电子式是_____ _____;其晶体类型是,晶体中存在的化学键有
⑶.C元素的最高价氧化物对应水化物与铜反应的化学方程式为:_____________ ___ _____。
配平方程式: Zn + HNO3— Zn(NO3)2 + N2 + H2O
下列是中学化学常见的物质
A.金刚石 B.HCl C.NaCl D.Na2 SO4 E.Na2S F .He G.N2
请用序号回答(1)-(4)题:
(1)这些物质中只含共价键的是
(2)既含离子键又含共价键的是
(3)固态时属于离子晶体的是
(4)熔化时需克服共价键的是
(5)试写出E. G的电子式:
用“>”、“<”回答下列问题:
①酸性:H3PO4H2SiO3 。H2CO3H2SiO3
②碱性:Mg(OH)2Ca(OH)2Mg(OH)2Al(OH)3
③气态氢化物稳定性;H2SH2O H2OHCl
④还原性: H2O HCl
HCl
已知: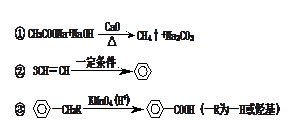
又知:⑴A、B、D、E、G、H都属于芳香烃,且对称性较高;
⑵1mol A、H被KMnO4(H+)氧化分别得2 mol F、2mol I;
⑶A、E、G、H遇Br2的CCl4溶液都不褪色;
⑷A、G、H含碳量相同:
⑸H侧链及I的苯环上的一卤代物都只有一种。
请根据下列转化关系回答相关问题: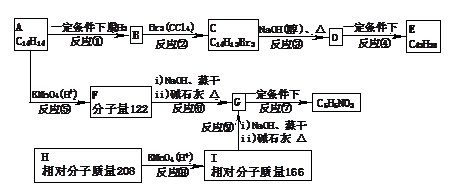
⑴请写出A、E、H结构简式:
AE H
⑵写出D与过量Br2的CCl4溶液反应的化学方程式:
⑶上述①~⑨的反应中,属于取代反应的是。