某溶液中含有Ba2+,Cu2+, Ag+,现用NaOH溶液、盐酸和Na2CO3溶液将这三种离子逐一沉淀分离。其流程图如所示
(1)沉淀的化学式(写出最佳答案):
沉淀1 ,沉淀3 ;
(2)写出溶液+B的离子方程式: 。
(每空1分,共6分)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是(写化学式)。
(2)写出并配平该反应的化学方程式:;
(3)发生氧化反应的物质是,反应中4mol的氧化剂能(填“失去”或“得到”)mol电子;
(4)反应中产生了11.2L(标准状况)的气体时,被还原的物质的质量为。
(每个方程式2分,其余每空1分,共8分)现有下列物质:①KI②铜③稀硝酸④NH3⑤NaHSO4⑥Ba(OH)2⑦氢氧化铁胶体⑧氨水
(1)按物质的分类方法填写表格的空白处(填物质编号)
| 分类标准 |
电解质 |
盐 |
非电解质 |
混合物 |
| 属于该类的物质 |
(2)上述某两种物质在溶液中可发生离子反应:H++OH-=H2O,写出该离子反应对应的化学方程式。
(3)物质①的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为。
下列关于各实验装置的叙述中不正确的是( )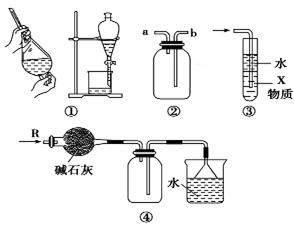
| A.装置①可用于分离C2H5OH和H2O的混合物 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
已知铜在常温下能被HNO3溶解,反应方程式为:
3Cu+8HNO3===3Cu(NO3)2+2NO↑+4H2O
(1)请将上述反应改成离子方程式
___________________________________________________________________
(2)上述反应中,氧化剂是 _____________,氧化产物是_____________。
(3)每2 molCu参加反应,转移的电子__________ 个,在反应的硝酸中没有参加氧化还原反应的硝酸占总硝酸的________________。
(10分)某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均己略去) 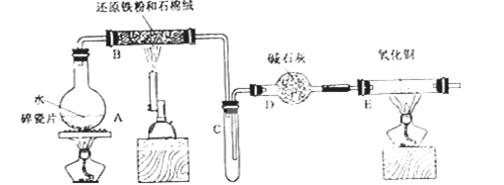
(1)装置B中发生反应的化学方程式是___________________________。
(2)装置E中的现象是________________________________________。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法:________________________。
(4)该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
滤液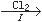 FeCl3溶液
FeCl3溶液 FeCl3·6H2O晶体
FeCl3·6H2O晶体
①步骤Ⅰ中通入Cl2的作用是____________________________________。
②该流程中需保持盐酸过量,主要原因是(结合离子方程式简要说明)_______________。