某温度时,AgCl(s)  Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。
Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。
下列说法正确的是
| A.加入AgNO3,可以使溶液由c点变到d点 |
| B.加入少量水,平衡右移,Cl-浓度减小 |
| C.d点没有AgCl沉淀生成 |
| D.c点对应的Ksp等于a点对应的Ksp |
氢氟酸(HF)是一种弱酸。25℃时,向20mL0.1mol/L氢氟酸中加入VmL 0.1mol/LNaOH溶液充分反应。已知:
HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H=-67.7kJ/mol
H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
根据题意,下列判断或结论正确的是
| A.氢氟酸的电离过程是吸热的 |
| B.当V=20时,溶液中:c(F-)<c(Na+)=0.1mol/L |
| C.当V<20时,溶液中离子浓度关系可能为:c(Na+)=c(F-) |
| D.当V>20时,溶液中离子浓度关系一定为:c(Na+)>c(F-)>c(OH-)>c(H+) |
某学习小组为研究电化学原理,设计如图装置。下列叙述不正确的是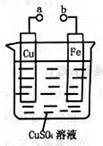
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为Cu2++2e- = Cu |
| C.a和b分别连接直流电源正、负极,Cu2+向铜电极移动 |
| D.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
CO(g)+H2O(g) H2(g)+CO2(g)△H﹤0,在其他条件不变的情况下,说法正确的是
H2(g)+CO2(g)△H﹤0,在其他条件不变的情况下,说法正确的是
| A.加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B.若在原电池中进行,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.改变压强,平衡不发生移动,反应放出的热量不变 |
实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42-= PbSO4+2e-
正极:PbO2+4H++SO42-+2e-= PbSO4+2H2O
今若制得Cl2 0.10 mol,这时电池内消耗的H2SO4的物质的量至少是
| A.0.025 mol | B.0.050 mol | C.0.10 mol | D.0.20 mol |
向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是 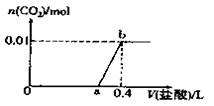
| A.在0-a范围内,只发生中和反应 |
| B.ab段发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑ |
| C.a=0.3 |
| D.原混合溶液中NaOH与Na2CO3的物质的量之比为1:2 |