在“质量守恒定律”的教学中,老师引导同学们进行“化学反应中反应物与生成物的质量关系”的实验探究,请你参与探究并回答有关问题:
(1)如图A、B所示,将锥形瓶(反应物未接触)放在天平上,右盘加砝码使之平衡,取下锥形瓶,将锥形瓶中两种物质混合,反应完全后将锥形瓶再放回天平左盘上。
①A瓶重新放回到天平上,天平 (填“能”或“不能”)保持平衡。
②B瓶重新放回到天平上,天平能否保持平衡? ,理由是 。
③从原子的角度分析“质量守恒定律” 。
(2)如上图C所示,用细线系住镁条使之平衡,然后在镁条一端用酒精灯加热。镁条在加热的条件下,能与空气中的氧气反应生成氧化镁。
①写出镁在空气中加热的文字表达式 。
②加热一段时间后,镁条 (填“能”或“不能”)保持平衡。
(3)某同学利用如图所示的装置测定空气中氧气的含量(体积分数)。他的操作过程如下(有100mL和500mL量筒供选用):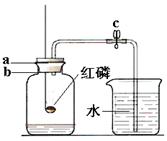
①检查整个装置的气密性后,将c处的止水夹夹紧,点燃红磷后,迅速插入左边的广口瓶中;
②待燃烧停止,整个装置冷却至室温后,将c处的止水夹打开。结果发现烧杯中的水进入到广口瓶中;
③待烧杯中的水不能再进入广口瓶后,打开广口瓶的橡胶塞,将广口瓶中的水全部倒入到100mL量筒中,测得其中水的体积为76ml。
④该同学又设法准确地测定了广口瓶中空气的体积,数据为400mL。
回答下列问题:①红磷燃烧时最明显的现象是___________________________;
②该同学测得的空气中氧气的体积分数为________%。与理论值21%相比较,产生误差的原因很可能是_____________________(导气管的体积可忽略不计)。
某初中化学兴趣小组的四位同学。往氢氧化钠溶液中滴加酚酞溶液时。发现溶液变成了红色,可是过了一会儿,红色就消失了,溶液恢复为无色,溶液的红色为什么会变成无色呢?他们对这一现象进行了探究,请你和他们一起完成下边的探究历程。
【提出猜想】
甲:可能是酚酞变质造成的;
乙:可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故;
丙:可能是酚酞与空气中的氧气发生反应,使红色消失;
丁:可能与氢氧化钠溶液浓度大小有关。
【理论分析】
(1)对于甲同学的猜想,你认为 ( 填“合理”或“不合理”).请写出你的理由: 。
(2)对于乙同学的猜想,大家认为是不正确的,因为氢氧化钠溶液虽然与空气中的二氧化碳反应,生成碳酸钠和水,但碳酸钠水溶液显碱性,由于溶液中有自由移动的 (写离子符号),所以红色不会消失。
【查阅资料】为了排除是酚酞溶液导致的原因,同学们决定重新配制酚酞溶液进行试验,他们在网络上查阅了资料,百度百科中对酚酞的描述如下表。
|
中文名 |
酚酞 |
结构式 |
|
|
外观 |
白色至微黄色结晶性粉末 |
||
|
常温下溶解性 |
<0.1g/100mL(水中) >5g/100mL(乙醇中) |
||
|
化学式 |
C20H14O4 |
(3)由上表可知,配制酚酞溶液的溶剂是 (选填“水”或“乙醇”).在检测溶液剂酸碱性的实验中,往待测溶液中滴入1﹣﹣2滴酚酞溶液即可,滴入过多的酚酞有可能出现白色沉淀的现象,该现象产生的原因是 。
【实验验证】
(4)如图,为了验证丙同学的猜想,四位同学在一支密封的装有NaOH 溶液的试管中,先通入密度比空气大的稀有气体,将试管内的空气排尽,随后注入新配制的酚酞溶液,观察到的现象依然是溶液先变成红色,过了一会儿红色消失,如图稀有气体应由导管口 (选填“a”或“b”)处通入。
(5)若丁同学的猜想正确,请你完成下列实验设计
|
实验方法 |
实验现象和结论 |
|
|
|
【应用拓展】
(6)从查阅百度百科资料知道,酚酞(H2In表示)其实是一种极弱的酸,其遇碱变红的变化表达式为:
H2In  In2﹣(红色)
In2﹣(红色)
根据上述信息,请写出H2In遇NaOH溶液变红的化学方程式: 。

氯气(Cl 2)是黄绿色气体,水溶液叫氯水,把品红试纸(染有品红的纸)伸入氯水中,品红褪色.
【发现问题】氯水中的哪些成分能使品红褪色呢?
【查阅资料】氯气溶于水,部分与水反应,方程式为Cl 2+H 2O=HCl+HClO.其中,HClO的名称叫次氯酸,是一种弱酸,具有强氧化性.
【做出猜想】
猜想1:是氯水中的水使品红褪色的;
猜想2:是氯水中的 使品红褪色的;
猜想3:是氯水中的盐酸使品红褪色的;
猜想4:是氯水中的次氯酸使品红褪色的.
【试验探究】
|
实验操作 |
实验现象 |
实验结论 |
|
①把品红试纸伸入水中 |
没有褪色 |
猜想1 |
|
②把品红试纸伸入干燥的氯气中 |
没有褪色 |
猜想2不成立 |
|
③ |
没有褪色 |
猜想3不成立 |
【实验结论】
综合分析判断:氯水中的 (填化学式)使品红褪色,具有漂白作用(能使品红等有色物质褪色).
【反思】
(1)HClO中氯元素的化合价为 价.
(2)氯水中加入AgNO 3溶液有白色沉淀生成,化学方程式为 .
(3)向氯水中滴加紫色石蕊试液,观察到的现象是 .
某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验。
(1)甲同学在烧杯中加入约15mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈
色。接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液变为无色,反应的化学方程式为 。
(2)甲、乙、丙同学对反应后溶液中的溶质成分进行探究。
【猜想与假设】反应后溶液中的溶质是什么?
猜想一:只有NaCl
猜想二:
猜想三:有NaCl和NaOH
上猜想中,直接可以排除的是 ,理由 。
【实验探究】
为了验证另外两种猜想,甲、乙、丙同学设计如下实验方案:
|
实验操作 |
实验现象 |
实验结论 |
|
|
甲同学方案 |
取少量反应后的溶液于试管中向试管中滴加AgNO 3溶液 |
有白色沉淀产生 |
猜想一成立 |
|
乙同学方案 |
取少量反应后的溶液于试管 中,向试管中加入 |
有气泡产生 |
猜想二成立 |
|
丙同学方案 |
取少量反应后的溶液于试管中,向试管中加入生锈的铁钉 |
|
猜想二成立 |
丙同学认为甲同学方案不合理,你认为理由是 。
【反思交流】
实验结束后,废液处理方法正确的是 (填序号)。
A.倒入下水道 B.倒入废液缸 C.带出实验室
小维与家人聚餐时,对火锅燃料"固体酒精"产生了好奇,于是他与同学对其成分进行如下探究。
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的。
(2)氯化钙、氯化钡溶液均呈中性。
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中氢氧化钠是否变质?
【作出猜想】猜想一:酒精中含有碳元素。
猜想二:固体酒精中氢氧化钠已变质。
【实验探究】(1)如图1所示进行实验,发现澄清石灰水 ,可得出酒精中含有碳元素的结论。
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现杯底有白色沉淀。取沉淀于试管中加入稀盐酸,固体溶解并有气泡产生,则生成气体的化学方程式 。
【实验结论】(1)酒精中含有碳元素。
(2)固体酒精中氢氧化钠已经变质。
【拓展延伸】为进一步确定固体酒精中是否还含有氢氧化钠,小维与同学继续探究。
(1)他另取少量固体酒精,加水溶解后,取上层清液,滴加酚酞溶液,酚酞溶液 ,于是得出固体酒精中还含有氢氧化钠。
(2)小维的同学认为他的实验不能证明固体酒精中一定有氢氧化钠剩余,理由是 。
(3)他们另取上层清液,加入足量的氯化钡溶液,充分反应后滴加氯化铁溶液,生成红褐色沉淀,他们一致认为固体酒精中氢氧化钠有剩余。
【反思交流】(1)实验中,加入足量氯化钡溶液的目的是 。
(2)实验室中氢氧化钠应 保存。

家庭厨房或卫生间的管道常被厨余垃圾或脱落的头发堵塞而令人烦恼.市面上有固态、液态两种管道疏通剂,研究小组购买了这两种管道疏通剂进行探究.
【查阅资料】
①固态管道疏通剂主要成分为NaOH、NaNO 3和铝粉.
②铝粉能与NaOH溶液反应并能放出热量,其化学方程式为:2Al+2NaOH+2H 2O=2NaAlO 2+3H 2↑.
③BaSO 4、BaCO 3都不溶于水,BaSO 4也不溶于酸.
探究一:
【提出问题】固态管道疏通剂能够疏通管道的原理是什么?
【实验验证】
|
操作 |
现象 |
解释与结论 |
|
将菜叶、头发、米饭等垃圾放入烧杯中,然后加入少量固态管道疏通剂,再加入 . |
烧杯中产生大量气泡,烧杯壁发热,垃圾翻动,一段时间后菜叶、米饭部分溶解并分散成小颗粒,头发变成碎屑. |
反应中产生的 使垃圾翻动. NaOH使垃圾分散成小颗粒,头发变成碎屑. |
【反思评价】经过大家讨论,认为固态管道疏通剂虽然能疏通管道,但使用过程中不安全,理由是 ;
目前超市出售更多的是液态管道疏通剂.液态管道疏通剂的成分主要是NaOH和一种钠盐.
探究二:
【提出问题】液态管道疏通剂中除NaOH以外,另一种钠盐是什么呢?
【猜想假设】这种钠盐是NaCl、Na 2SO 4、Na 2CO 3、NaNO 3中的一种.
【实验验证】(不考虑疏通剂中其它成分对实验的影响)
|
操作 |
现象 |
结论 |
|
取少量液态疏通剂加入试管中,滴加 溶液. |
产生白色沉淀 |
该钠盐是Na 2SO 4,写出该反应的化学方程式: . |
【提出质疑】同学们认为该实验不能证明这种钠盐一定是Na 2SO 4,理由是 ,
请你补充一个实验证明该钠盐是Na 2SO 4: ;
【拓展延伸】NaOH有强烈的腐蚀性,能腐蚀皮肤和衣物等,但管道疏通剂正是利用了它的腐蚀性,将"弊"变"利".请你再举出一个利用物质的"弊"为生活服务的例子: .