为研究草酸亚铁晶体(FeC2O4•2H2O,相对分子质量是180)分解的产物,在实验室里称取一定量的草酸亚铁晶体,利用下列装置进行实验。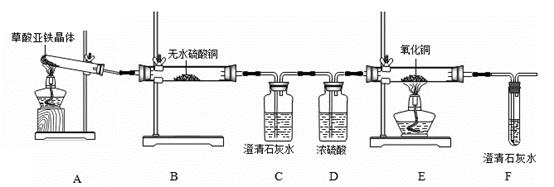
①实验过程中观察到B中白色无水CuSO4变成蓝色,C、F中澄清石灰水变浑浊,则E中现象是 (9) (填实验现象)。分解产物中有CO气体,还有 (10) 。
②若该实验过程中E装置内有6.4g铜生成,计算有多少物质的量的氧化铜参加了反应?(写出反应的化学方程式,列出计算步骤!)
(11)写方程式:
(12)计算步骤:
③为验证CO的性质,收集装置D后的气体于集气瓶中,将点燃的木条伸入集气瓶中(如右图),在此过程中的实验现象是(13) (选填编号)。
A.木条熄灭 B.木条继续燃烧
C.瓶口产生淡蓝色火苗 D.发生爆炸
④进行上述实验时,先点燃A处的酒精灯,一段时间后再点燃E处的酒精灯,原因是(14) 。
⑤若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需在C和D装置之间增加如图所示的洗气瓶,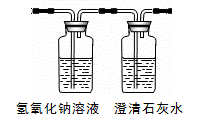
其中氢氧化钠溶液中发生的反应方程式是:(15) ;
澄清石灰水起到的作用是:(16) 。
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_____________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO___________________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
将气体通入澄清的石灰水中 |
澄清石灰水变浑浊 |
| ② |
将带火星的木条伸入该气体中 |
带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有_________。
(2)由实验②_____________(填“能”或“不能”)确定该气体中不含氧气,理由是_____________________________________________________________。
探究二:维C泡腾片溶液的酸碱性。
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显_________性。
在实验室,有硫酸铜、碳酸钙、碳酸钠、氢氧化钠、氢氧化钙五种物质(均为纯净物)失去标签,它们均为白色粉末。现将药品分别标记为A、B、C、D、E,化学老师让化学实验小组的同学鉴别出这些物质。
【查阅资料】白色的硫酸铜粉末遇水变为蓝色
【实验探究】化学实验小组的同学鉴别实验过程记录如下步骤1:取五种白色粉末各一药匙,分别放入五支洁净的试管中,各加蒸馏水2mL。振荡后静置。五支试管底部均有固体存在,只有盛放E的试管中液体呈蓝色, 其他均呈无色。
步骤2:取B、C、D的上层清液滴加稀盐酸,只有B的试管中有气泡产生,其他均无明显现象。
步骤3:取A、C、D的上层清液放入试管中,分别滴加无色酚酞,A、C显红色。
请根据该学生的实验过程,回答下列问题:
(1)由步骤1得出E为;
(2)步骤3中,D的现象是;
(3)根据该化学小组的实验,除E外其余四种白色粉末有部分也可以确定,分别是;(写代号及其对应物质的化学式)
(4)对尚未鉴别出来的物质,请设计实验进行确定,并填入下表:
| 实验操作 |
实验现象及结论 |
【实验反思】“四支试管底部均有固体存在”,与化学小组同学预测的只有一只试管中有固体体存在,其他试管中均为澄清溶液”的现象不同,其原因可能是。
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小滨同学设计了实验,以探究碳酸氢钠的化学性质.
【探究实验1】碳酸氢钠溶液的酸碱性
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞实验,震荡.
现象:溶液变成浅红色.由此得出结论 ;
【探究实验2】能与酸反应
【实验方案】取少量该固体加入试管中,滴加稀盐酸,现象为 ;
【探究实验3】碳酸氢钠的热稳定性
【实验方案】用如图所示装置进行实验
现象:充分加热后,大试管口有.出现,管底有白色固体残留,
小试管中的现象..
结论:碳酸氢钠受热能生成二氧化碳、水和一种白色固体.
验证:(1)请你帮小滨设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH(所选试剂不能用酸).
| 步骤 |
现象 |
结论 |
| 取样于试管中,往试管中滴加 |
(2)写出碳酸氢钠受热分解的化学方程式 ;
【拓展应用】试说出碳酸氢钠在日常生活中的一种用途 .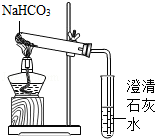
针对利用双氧水和二氧化锰制取氧气的实验,请结合下图所示常用仪器和装置,回答有关问题: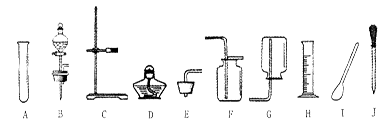
(1)配制溶液:若配制60g溶质质量分数为5%的双氧水溶液,需要30%的双氧水溶液g,需要加入水的体积为mL。在量取水的操作中,当水面接近所需刻度时,应改用(填仪器名称)加水至所需刻度。
(2)贴标签:将配制好的溶液装入试剂瓶中,请在如图所示的标签内填入试剂瓶所贴标签的内容。
(3)选仪器:用双氧水和二氧化锰制取氧气,该反应的化学方程式是,其发生装置和收集装置可选择上图中的(填序号)组合,从所选的装置组合中选择一种仪器,写出它的名称,简要说出它的用途。
(4)实验步骤:
①检查氧气发生装置的。
②先往容器中装入固体粉末,具体的操作方法是,再装入液体试剂。
③收集气体,并用带火星的木条来验满。验满的方法是利用氧气具有的性质。
(5)回收处理:把氧气发生装置容器内的残留物经(写操作名称)、洗涤、干燥回收二氧化锰。
实验室有一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4、NH4HCO3和尿素[CO(NH2)2]中的一种。请你完成以下探究:
【猜想】猜想①:该化肥是NH4Cl,
猜想②:该化肥是,
猜想③:该化肥是NH4HCO3,
猜想④:该化肥是尿素。
【实验探究】
(1)取少量样品在研钵中与熟石灰研磨,有刺激性气味的气体放出,证明猜想不成立;写出其中一种化肥发生该反应的化学方程式:。
(2)如(图1),另取少量样品于试管中,滴加适量水振荡,再选(图2)中溶液滴入试管中,若无气泡放出,则猜想不成立。
(3)在步骤(2)的试管中再滴入(图2)中的溶液,若,则猜想①成立;若,则猜想②成立,其反应的化学方程式为。