(8分) 已知600℃时,在2L密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g) 2SO3(g) △H= -197 kJ·mol-1反应过程中SO2、O2、SO3物质的量变化如图所示。
2SO3(g) △H= -197 kJ·mol-1反应过程中SO2、O2、SO3物质的量变化如图所示。
(1)反应开始到20min时,用SO3表示的反应平均速率为 。
(2)10min、15min、20min曲线均出现拐点,10min时曲线变化的原因可能是 (填选项标号);20min时,曲线发生变化是因为 (填选项标号)。
A.升高温度
B.降低压强
C.加入氧气
D.加入SO3
E.加入催化剂
(3)下列描述能说明该反应达到平衡状态的是 。
A.混合气体的总质量不随时间的变化而变化
B.SO2的转化率达到最大,且保持不变
C.化学反应速率v(O2)="v" (SO3)
D.保持温度和容积不变,混合气体的总压强不随时间的变化而变化
液晶高分子材料应用广泛。新型液晶基元------化合物Ⅳ的合成线路如下:
(1)化合物Ⅰ的分子式为__________ ,1mol化合物Ⅰ完全燃烧消耗_____molO2。
(2)CH2=CH-CH2Br与NaOH水溶液反应的化学方程式为_____(注明条件)。
(3)写出符合下列条件的化合物Ⅰ的同分异构体的结构简式。
I. 苯环上有3个取代基 II.苯环上一溴代物只有2种III.能发生银镜反应
(4)下列关于化合物Ⅱ的说法正确的是_______(填字母)。
| A.属于烯烃 | B.能与FeCl3溶液反应呈紫色 |
| C.一定条件下能发生加聚反应 | D.最多能与4molH2发生加成反应 |
(5)反应③的反应类型是____________。在一定条件下,化合物 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ。Ⅴ的结构简式是______________。
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ。Ⅴ的结构简式是______________。
资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品。(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式如下:
6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ,ΔH=—76.0 kJ·mol-1,该反应中每放出38 kJ热量,转移电子的物质的量为mol.
(2)在一定条件下,二氧化碳转化为甲烷的反应如下:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH<0
CH4(g)+2H2O(g) ΔH<0
①向一容积为2L的恒容密闭容器中充人一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO20.2mol·L—1,H20.8mol·L—1, CH40.8mol·L—1,H2O1.6mol·L—1,起始充CO2和H2的物质的量分别为、。CO2的平衡转化率为
②现有两个相同的恒容绝热(与外界没有热量交换)密闭容器I、II,在I中充人1 mot CO2,和4 molH2,在II中充人1 mol CH4和2 mol H2 O(g) , 300℃下开始反应。达到平衡时,下列说法正确的是(填字母)。
| A.容器I、II中正反应速率相同 |
| B.容器I、II中CH4的物质的量分数相同 |
| C.容器I中CO2的物质的量比容器II中的多 |
| D.容器I中CO2的转化率与容器II中CH4的转化率之和小于1 |
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示: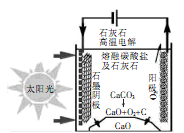
①上述生产过程的能量转化方式是
②上述电解反应在温度小于900 0C时进行碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为,阴极的电极反应式为
溴化钙(CaBr2·2H2O)是一种白色晶体,易溶于水,有很强的吸湿性,是光敏纸矿泉水和灭火剂的重要成分,在医药上用作治疗神经衰弱等的药物,也用作化学分析。用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下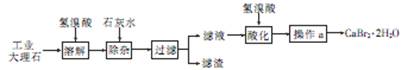
回答下列问题
(1)溶解时发生的主要反应的离子方程式为
(2)除杂步骤控制溶液的pH约为8.0的目的是,
(3)滤液用氢溴酸酸化的目的是,操作a主要包括,和过滤
(4)制得的溴化钙晶体可以通过如下步骤测定其纯度:
①称取5.00g溴化钙晶体样品,②溶解;③滴入足量Naa2CO3溶液,充分反应后过滤,④烘干、冷却;⑤称量。若得到2. 00 g碳酸钙,则样品的纯度为
(5)溴化钙晶体中溴离子和钙离子的检验
①将少量溴化钙晶体溶于水,加入硝酸酸化的AgNO3溶液,实验现象为,发生反应的离子方程式为
②将少量溴化钙晶体溶于水,滴加草酸钠溶液,实验现象为,发生反应的离子方程式为
绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途,在某些食品中可取代或部分取代目前常用的人工合成的抗氧化剂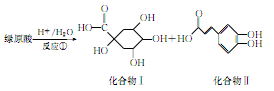
(1)化合物I的分子式为,反应①的反应类型为
(2)1 mol化合物I与足量金属钠反应生成标准状况下氢气的体积为
(3)写出化合物II与足量浓溴水反应的化学方程式
(4)1mol化合物II与足量的试剂X反应得到化合物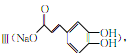 ,则试剂X是
,则试剂X是
(5)化合物IV有如下特点①与化合物II互为同分异构体;②遇 FeCl3溶液不显色;③1 mol化合物IV与足量银氨溶液反应生成4molAg;④1 mol化合物IV与足量NaOH溶液反应消耗4 mol NaOH;⑤核磁共振氢谱有4组峰,且峰面积之比为3:2:2:1,写出化合物IV所有可能的结构简式:
黄铜矿(CuFeS2)是制铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是(填元素符号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是(填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82-+2I-=2SO42-+I2
通过改变反应途径,Fe3+可催化上述反应。试用离子方程式表示Fe3+对上述反应的催化过程。、
。
(不必配平,每空1分)。
(4)利用黄铜矿冶炼铜产生的炉渣(Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得。
据以上信息回答以下问题:选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液碘水
所选试剂为。证明炉渣中含有的实验现象为
。