钛(Ti)被称为继铁、铝之后的第三金属,江西省攀枝花和西昌地区的钒钛磁铁矿储量十分丰富。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。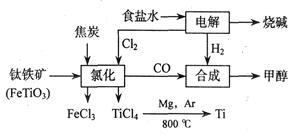
(1)电解食盐水时,总反应的离子方程式_____。
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式___________________。
(3)已知:①Mg(s)+Cl2(g)=MgCl2(s);ΔH=-641 kJ·mol-1
②Ti(s)+2Cl2(g)=TiCl4(s);ΔH=-770 kJ·mol-1
则2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);ΔH____________________
反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是_________________。
2MgCl4+Ti在Ar气氛中进行的理由是_________________。
(4)在上述产业链中,合成96t甲醇理论上需额外补充H2__________t(不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是____________________________________________________________。
在一定条件下,乙烯和乙烷都能制备氯乙烷(CH3CH2Cl)。据此请回答:
⑴、由乙烷制备氯乙烷的化学方程式为_________________,该反应属于________反应。
⑵、由乙烯制备氯乙烷的化学方程式为_________________,该反应属于________反应。
⑶、比较两种方法,第_____种方法较好,其原因是__________________________。
在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2.X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的化学式是 ,X与氢元素形成的化合物的电子式是;
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是 ;
D与E能形成一种非极性分子,该分子的结构式为 ;
D所在族元素的氢化物中,沸点最低的是 .
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价键;
W与Z能形成一种新型无机非金属材料,其化学式是 .
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃, R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为 ;
铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关。已知铁与冷的稀HNO3反应时,主要还原产物为NO气体;与热的稀HN03反应时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+。现有铁与稀 HNO3的作用,请分析下图,回答有关问题。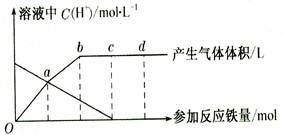
假设曲线的各段内只有一种还原产物,。
(1)0点到a点的还原产物是 。
(2)a点到b点的还原产物是____,其原因是 。
(3)试完成b点到c点的反应方程式:
口Fe+口HNO3——口Fe( NO3)3+口[ ]+口H20。
(4)反应过程中,到达点时,HN03已完全反应。
(5)已知达到d点时反应结束,此时溶液中的主要阳离子是 。
(6)c点和d点参加反应的铁的物质的量之比是 。
甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。x、 A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,G的焰色反应为黄色。在一定条件下,各物质相互转化关系如下图: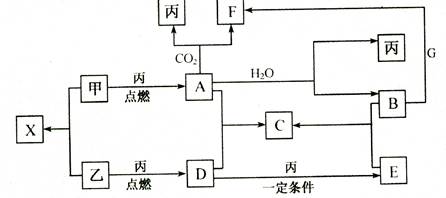
(1)用化学式表示:丙为 ,C为
(2)X的电子式为 。
(3)写出A与H2O反应的化学方程式:
(4)写出B与G溶液反应的离子方程式:
某原电池装置中盛有NaOH浓溶液,若分别向 (填“正”或“负”,下同)极通入可燃性气体,向 极通入O2,则电路中就有电流通过,电流方向由极流向极,溶液中OH–向极移动。