软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO等杂质,工业上用软锰矿制取MnSO4·H2O的流程如下: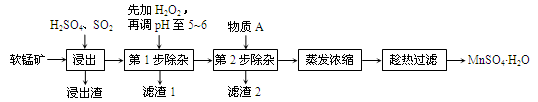
已知:Fe3+、Al3+、Mn2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、10.4、12.4;温度高于27℃时,MnSO4的溶解度随温度的升高而逐渐降低。
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为________。
(2)“浸出”过程中Fe2O3转化为Fe3+和Fe2+,相关反应的离子方程式为________。
(3)“滤渣1”的主要成分是__________,“调pH至5~6”所加的试剂是_________(填“石灰水”或“稀硫酸”)。
(4)根据下表数据,选择“第2步除杂”所加的物质A(由一种阳离子和一种阴离子组成),物质A的化学式为________。
 阴离子 阴离子Ksp  阳离子 |
CO32- |
F- |
OH- |
| Ca2+ |
5.0×10-9 |
1.5×10-10 |
4.7×10-6 |
| Mg2+ |
3.8×10-6 |
7.4×10-11 |
5.6×10-12 |
| Mn2+ |
2.2×10-11 |
5.3×10-3 |
2.1×10-13 |
| Zn2+ |
1.2×10-10 |
3.0×10-2 |
6.9×10-17 |
(5)采用“趁热过滤”操作的原因是________。
药物萘普生具有较强的抗炎、抗风湿和解热镇痛作用,其合成路线如下: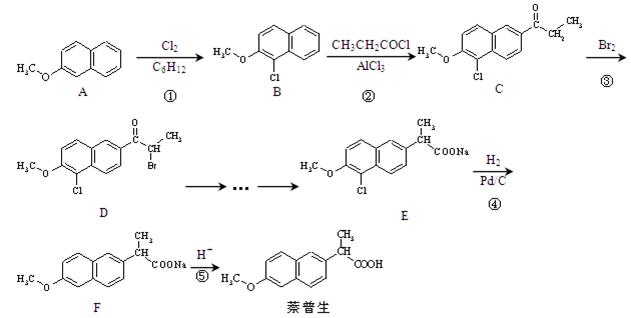
⑴写出萘普生中含氧官能团的名称: 和 。
⑵物质B生成C的反应类型是 反应。
⑶若步骤①、④省略,物质A与CH3CH2COCl直接反应除生成G(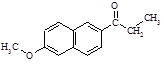 )外,最可能生成的副产物(与G互为同分异构体)的结构简式为 。
)外,最可能生成的副产物(与G互为同分异构体)的结构简式为 。
⑷某萘(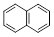 )的衍生物X是C的同分异构体,分子中含有2个取代基,且取代基在同一个苯环上;X在NaOH溶液中完全水解后,含萘环的水解产物的核磁共振氢谱有5个峰。写出X可能的结构简式: (任写一种)。
)的衍生物X是C的同分异构体,分子中含有2个取代基,且取代基在同一个苯环上;X在NaOH溶液中完全水解后,含萘环的水解产物的核磁共振氢谱有5个峰。写出X可能的结构简式: (任写一种)。
⑸已知:RCOOH RCOCl。根据已有知识并结合相关信息,写出以苯和乙酸为原料制备
RCOCl。根据已有知识并结合相关信息,写出以苯和乙酸为原料制备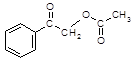 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
CH2=CH2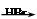 CH3CH2Br
CH3CH2Br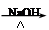 CH3CH2OH
CH3CH2OH
聚碳酸酯无色透明,具有优异的抗冲击性,能用于制造宇航员的面罩、智能手机机身外壳等。双酚化合物是合成聚碳酸酯的单体之一,某种双酚化合物G的合成路线如下:
(1)G中所含的官能团有________________;B的核磁共振氢谱有 个峰。
(2)写出反应类型:反应 ① ___________;反应 ③ ____________。
(3)写出A的名称 ______________;F的结构简式 ______________。
(4)写出反应 ④ 的化学方程式_______________________________________。
(5)C有多种同分异构体,写出同时满足下列条件的同分异构体的结构简式_____________。
(I)属于α-氨基酸,且苯环上有三个互为间位的取代基
(II)与FeCl3溶液作用无显色现象
(III)1 mol该同分异构体与足量NaOH溶液反应时,最多能消耗3 mol NaOH
有机物A的分子式为C9 H10 O2,A在光照条件下生成的一溴代物B,可发生如下转化关系(无机产物略):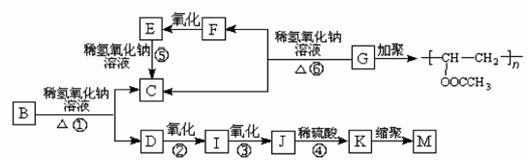
其中K物质与氯化铁溶液发生显色反应,且环上的一元取代物只有两种结构。
已知:①当羟基与双键碳原子相连时,易发生如下转化:RCH=CHOH→RCH2CHO;
② —ONa连在烃基上不会被氧化。
请回答下列问题:
(1)F与I中具有相同的官能团,检验该官能团的试剂是 。
(2)上述变化中属于水解反应的是 (填反应编号)。
(3)写出结构简式,G: ,M: 。
(4)写出下列反应的化学方程式:反应①: ,K与少量的氢氧化钠溶液反应: 。
(5)同时符合下列要求的A的同分异构体有 种。
I.含有苯环Ⅱ.能发生银镜反应和水解反应
Ⅲ.在稀氢氧化钠溶液中,1mol该同分异构体能与1mol NaOH反应
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜。E的一种合成路线如下: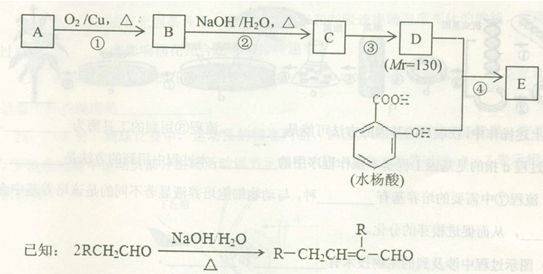
请回答下列问题:
(1)A是分子式为C4H10O的一元醇,分子中只有一个甲基。F与A互为同分异构体,F的核磁共振氢谱图有2组峰,且峰面积比为9:1。则F与浓HBr溶液共热生成有机物的结构简式为 。
(2)B能与新制的Cu(OH)2悬浊液发生反应,该反应的化学方程式为 。
(3)C中所含官能团的名称为 ,若要检验C中所含官能团,一次取样检验,按使用试剂的先后顺序,下列选项中组 (填字母编号)更为合理。
a.银氨溶液、溴水 b.溴水、银氨溶液
c.银氨溶液、稀盐酸、溴水 d.溴水、氢氧化钠溶液、银氨溶液
(4)第③步的反应类型为 。
(5)同时符合下列条件的水杨酸的同分异构体有 种。
a.分子中含有6个碳原子在同一条直线上
b.分子中所含官能团包括水杨酸具有的含氧官能团
共聚法可改进有机高分子化合物的性质,高分子聚合物P的合成路线如下: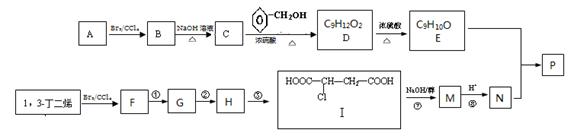
(1)A的结构式为________________ ,C的名称为
(2)D中含有的官能团的名称
(3)由F经①~③合成I,F可以使溴水褪色.反应①的化学方程式是 。
反应②的反应类型是 反应③的反应试剂是 。
(4)下列说法正确的是 。
a.C可与水任意比例混合
b.A与1,3-丁二烯互为同系物
c.由I生成M时,1mol I最多消耗3molNaOH
d.N不存在顺反异构体
(5)写出由D生成E的化学方程式 。
(6)E与N等物质的量发生共聚反应生成P,则P的结构简式为 。
(7)E有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式 。
a.苯环上有两个取代基
b.能使FeCl3液显紫色
c.1mol该有机物与浓溴水反应时能消耗4molBr2