某课外小组探究钠、铝、铁、铜单质还原性强弱及其相关化学性质,做了如下实验:
| 实验1 |
常温时取四种金属少量分别放入装有蒸馏水的试管中 |
| 实验2 |
再取少量铝、铁、铜分别放入装有稀硫酸的试管中 |
(1)实验1中能发生反应的离子方程式 。
(2)实验2中能够判断出铝、铁、铜还原性强弱的现象是 。
结论:由实验1、2得出四种金属的还原性强弱顺序为 ;请从原子结构角度解释钠的还原性强于铝 。
(3)为确认实验2反应后溶液中的金属阳离子,再进行实验:
①取Al反应后的溶液加入过量的NaOH溶液,写出反应的离子方程式 。
②一段时间后,取Fe反应后的溶液,检验Fe2+方法正确的是 。
a.滴加KSCN溶液,无明显变化,再加入少量氯水,溶液变红
b.滴加K3[Fe(CN)6]溶液,有蓝色沉淀产生
c.滴加NaOH溶液,产生的白色沉淀迅速变成灰绿色,最终变成红褐色
(4)在实验2中,铝、铁反应现象的差异并不是很明显,有同学建议再设计一种实验来证明这两种金属的还原性关系,请设计一种实验方案 。
(5)在实验过程中,还有同学为了验证铁与铜的还原性,用铁、铜、导线、烧杯、氯化铁溶液设计了原电池装置。
①画出原电池的装置图 。
②该电池的正极反应为 。
50ml0.50mol•L﹣1盐酸与50mL0.55mol•L﹣1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
(1)从实验装置上看,有两处缺点,其一是有处错误安装会导致热量散失较大,应该加 ,其二尚缺少一种玻璃仪器是 。
(2)若操作时分几次注入反应液,求得的反应热数值 (填“偏大”“偏小”或“无影响”).
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会 (填“偏大”、“偏小”或“无影响”).
(4)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2﹣t1分别为①2.2℃②2.4℃③3.4℃,则最终代入计算式的温差均值为 ℃
高锰酸钾在实验室和工农业生产中有广泛的用途,实验室以二氧化锰为主要原料制备高锰酸钾,其部分流程如下:
Ⅰ(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是 (用化学程式表示)。
(2)第④步通人适量CO2,发生反应生成KMn04和Mn02和碳酸盐,则发生反应的离子方程式为______________________。
(3)第⑥步加热浓缩至液面有细小晶体析出时,停止加热,冷却结晶、过滤、洗涤、干燥,干燥过程中,温度不宜过高,其原因是_____________________
(4)H2O2和KMn04都是常用的强氧化剂,若向H2O2溶液中滴加酸性高锰酸钾溶液,则酸性高锰酸钾溶液会褪色,该反应中氧化产物与还原产物的物质的量之比为 。
Ⅱ.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质。
(5)若从左端分别通人SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);
(6)若装置B中装有5.0 mL l.0 mol/L的碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2 mol电子,该反应的化学方程式为
(7)探究SO2的性质时,E装置中以NaOH溶液吸收尾气,实验结束后,E装置中可能含有的溶质为___________________(以化学式作答).
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为10lkPa,温度为0℃)。
(1)若在烧瓶中放入1.30g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的适宜规格是___________(以序号作答)。
A.200 mL B.400 mL C.500mL
(2)若1.30g锌粒完全溶解,氢氧化钠洗气瓶增重l.28g ,则圆底烧瓶中发生反应的化学方程式为: 。
(3)若烧瓶中投入a g锌且完全反应,氢氧化钠洗气瓶增重b g。量气瓶中收集到VmL气体,请写出a、b、v的代数关系式:____________________________
(4)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反 应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中,n(H2)/n(SO2)= ____________ ___(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,n(H2)/n(SO2)的数值将 (填偏大、偏小或无影响)
(5)反应结束后,为了准确地测量气体体积,量气管在读数时应注意:
① ② ③
[实验化学]
三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂。实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:
 |
物质 |
相对分子质量 |
密度/g·cm-3 |
沸点/℃ |
水中溶解性 |
| 甘油 |
92 |
1.2636 |
290(分解) |
溶 |
|
| 乙酸 |
60 |
1.0492 |
118 |
溶 |
|
| 三乙酸甘油酯 |
218 |
1.1596 |
258 |
不溶 |
实验步骤:
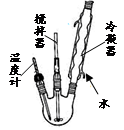
步骤1.在500mL反应器中加入200g冰醋酸,92g甘油和100mL苯,开动搅拌器,慢慢从插温度计口加入3mL浓硫酸后,缓缓加热并回流1h,停止加热。
步骤2.用5%碳酸钠溶液洗涤,再用水洗涤,最后加入无水氯化钙。
步骤3.先进行常压蒸馏收集75~85℃馏分。
步骤4.将常压馏分再进行减压蒸馏,收集128~131℃/933Pa馏分,最终得产品176g。
(1)步骤1先开搅拌器后加浓硫酸的目的是 ;冰醋酸过量的目的是 。
(2)用5%碳酸钠溶液洗涤的主要目的是 ;加无水氯化钙的目的是 。
(3)最后用减压蒸馏而不用常压蒸馏其原因是 。
(4)本次实验产率为 。
焦亚硫酸钠(Na2S2O5)在食品加工中常用作防腐剂、漂白剂和疏松剂。焦亚硫酸钠为黄色结晶粉末,150℃时开始分解,在水溶液或含有结晶水时更易被空气氧化。实验室制备焦亚硫酸钠过程中依次包含以下几步反应:
2NaOH + SO2 = Na2SO3 + H2O……(a)
Na2SO3+ H2O + SO2 = 2NaHSO3 ……(b)
2NaHSO3 Na2S2O5 + H2O……(c)
Na2S2O5 + H2O……(c)
实验装置如下:
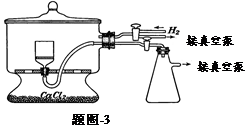
(1)实验室可用废铝丝与NaOH溶液反应制取H2,制取H2的离子方程式为 。
(2)题图-1装置中,导管X的作用是 。
(3)通氢气一段时间后,以恒定速率通入SO2,开始的一段时间溶液温度迅速升高,随后温度缓慢变化,溶液开始逐渐变黄。“温度迅速升高”的原因为 ;
实验后期须保持温度在约80℃,可采用的加热方式为 。
(4)反应后的体系中有少量白色亚硫酸钠析出,参照题图-2溶解度曲线,除去其中亚硫酸钠固体的方法是 ;然后获得较纯的无水Na2S2O5应将溶液冷却到30℃左右抽滤,控制“30℃左右”的理由是 。
(5)用题图-3装置干燥Na2S2O5晶体时,通入H2的目的是 ;真空干燥的优点是 。
(6)测定产品中焦亚硫酸钠的质量分数常用剩余碘量法。已知:S2O52-+2I2+3H2O=2SO42-+4I-+6H+;2S2O32-+I2 = S4O62-+2I-
请补充实验步骤(可提供的试剂有:焦亚硫酸钠样品、标准碘溶液、淀粉溶液、酚酞溶液、标准Na2S2O3溶液及蒸馏水)。
①精确称取产品0.2000g放入碘量瓶(带磨口塞的锥形瓶)中。
②准确移取一定体积和已知浓度的标准碘溶液(过量)并记录数据,在暗处放置5min,然后加入5mL冰醋酸及适量的蒸馏水。
③用标准Na2S2O3溶液滴定至接近终点。④ 。 ⑤ 。
⑥重复步骤①~⑤;根据相关记录数据计算出平均值。