某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。该小组同学进行了如下探究.
(1)写出铁丝在氧气中燃烧的文字表达式: 。
(2)探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图)由此可知:蜡烛燃烧产生的火焰是由 (填:“固态”或“气态”)物质燃烧形成的.
(3)探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
| 物质 |
熔点/℃ |
沸点/℃ |
燃烧时温度/℃ |
| 石蜡 |
50~70 |
300~550 |
约600 |
| 铁 |
1535 |
2750 |
约1800 |
| 钠 |
97.8 |
883 |
约1400 |
由上表可知:物质燃烧能否产生火焰与其 (填:“溶点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时, (填:“有”或“没有”)火焰产生.
(4)木炭在氧气中燃烧没有火焰,但生活中木炭燃烧时往往会产生火焰,其原因可能是 .
(1)用石蕊染成紫色的干燥纸花,进行如下操作,能够观察到纸花变红的是.
(2)下列
是探究物质性质的实验:
二氧化碳是否可以溶于水,很难直接观察到现象,可以通过
中塑料瓶的变化来间接感知.同样,研究氢氧化钠溶解于水时是吸热还是放热,可利用密闭的广口瓶内的变化引起
形管内水位的变化,若(填
或
)处的水位升高,则是放热.
(3)一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.下表是实验中可能出现的现象与对应结论,请你填写下表中空白处的相关内容:
| 现象 |
结论 |
| |
含 |
| 溶液颜色无明显变化,有黑色不溶物 |
只含 |
通过实验及分析,确定该粉末为氧化铜和碳粉混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如图所示实验:
①试管
中的化学方程式为.
②氧化铜和碳反应属于反应.(填基本反应类型)
③最能说明
试管中氧化铜和碳已完全反应的实验现象是.
人教版新课标化学教材九年级上册(2012教育部审定)"分解过氧化氢制氧气的反应中二氧化锰的催化作用",以及"寻找新的催化剂"研究性实验,引起了化学探究小组的兴趣.
【实验探究】
| 实验步骤 |
实验现象 |
| Ⅰ.分别量取5
5%过氧化氢溶液放入
、
两支试管中,向
试管中加入
氧化铁粉末,并分别在
、
两支试管中插入带火星木条,观察现象. |
试管中产生气泡,带火星木条复燃,
试管中无明显现象 |
| Ⅱ.待
试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象. |
试管中均产生气泡,带火星木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为
. |
|
| Ⅳ.分别量取5
5%过氧化氢溶液放入
、
两支试管中,向
试管中加入
氧化铁粉末.向
试管中加入
二氧化锰粉末,观察现象. |
【实验结论】
(1)
中产生的气体是;
(2)实验Ⅱ、Ⅲ证明:氧化铁的和在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)写出氧化铁催化过氧化氢分解的化学方程式.
【实验评价】
(1)设计实验Ⅳ的目的是;
(2)若实验Ⅳ观察到
试管中产生气泡的速率更快,由此你可以得到的结论是.
【实验拓展】
查阅资料得知:
、
、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂.下列有关催化剂的说法中正确的是.
| A. |
只能作为氧化氢溶液分解的催化剂 |
B. |
同一个化学反应可以有多种催化剂 |
C. |
催化剂只能加快化学反应的速率 |
D. |
用作催化剂的物质不可能是其它反应的反应物或生成物 |
E. |
酶是一种重要的生物催化剂,它属于糖类 |
化学兴趣小组同学发现实验台上按如图所示顺序摆放着6瓶不同的无色溶液(如图所示:A、B、C、D、E、F代表对应的溶液).其中E溶液的试剂瓶标签破损.为此,他们做了如下探究: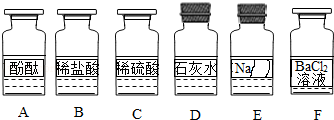
【提出问题】E溶液的成分是什么?
【初步判断】根据受损标签及实验室药品分类摆放原则,E溶液不可能是(填序号).①酸;②碱;③盐.
【提出猜想】猜想Ⅰ:
溶液;猜想Ⅱ:
溶液;猜想Ⅲ:
溶液;猜想Ⅳ:溶液(任写一种).
【设计并实验】兴趣小组的同学为验证"猜想Ⅱ"是否正确,设计并完成如下表所示实验.
| 实验方案 |
实验一 |
实验二 |
实验三 |
| 实验操作 |
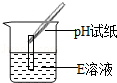 |
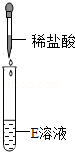 |
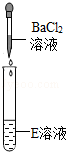 |
| 实验现象 |
试纸变色,对照比色卡,pH>7 |
有无色无味气体产生 |
|
| 实验结论 |
猜想Ⅱ正确 |
【分析与推理】
①完成"实验一"后,李成同学即认为"猜想Ⅰ"正确,张平同学认为"猜想Ⅰ"不一定正确,他的理由是.
②何刚同学认为只需要完成"实验二"即可得出"猜想Ⅱ"正确的结论,你认为该说法(填"合理"或"不合理"),理由是.
③请写出"实验三"中发生反应的化学方程式.
【反思与评价】
经过讨论,同学们认为"实验一"存在明显操作错误,该错误是;观察发现D、E试剂瓶的瓶塞是橡胶塞,使用橡胶塞的原因是.
某研究学习小组对“NaOH溶液与稀H2SO4溶液是否恰好反应”进行实验探究.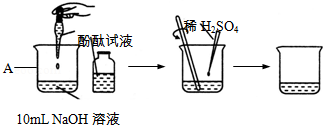
(1)如图是类似教材所示酸与碱反应的实验过程.
①图中仪器A的名称是 .
②向A中加入10mLNaOH溶液,并滴入3滴酚酞试液,再向其中慢慢滴入稀硫酸,并用玻璃棒不断 ,使溶液混合均匀,直至溶液的颜色由红色恰好变成 色为止,表明两者发生了反应,该反应的化学方程式为 .
(2)为探究上述酸碱反应后,硫酸是否过量.设计了如下两种方法:
方法①:取少量反应的溶液,用pH试纸检验,测得pH<7,表明硫酸过量.
方法②:取少量反应的溶液,向其中滴加适量的BaCl2溶液,可观察到有白色沉淀产生,表明硫酸过量.
上述两种方法中,你认为正确的是方法 (选填“①”或“②”).请用文字说明另一种方法不合理的原因 .
查阅资料得知:氢氧化钠溶液中 含有
,
,
.某化学兴趣小组同学欲探究氢氧化钠溶液中哪一种粒子能使无色酚酞试液变红,做了三个实验设计:
实验一:在第一支试管中加入约2ml蒸馏水,再滴入几滴无色酚酞试液,观察实验现象.
实验二:在第二支试管中加入约2ml,5%
(pH=7)溶液,再滴入几滴无色酚酞试液,观察实验现象.
实验三:在第三支试管中加入约2ml,5%
溶液,再滴入几滴无色酚酞试液,观察实验现象.
根据上述实验探究回答下列问题:
(1)实验一观察到的现象是,得出的结论是.
(2)实验二观察到的现象是,得出的结论是:
不能使无色酚酞试液变红色.
(3)实验三观察的现象是,得出的结论是.
(4)拓展应用:向滴加2﹣3滴无色酚酞试液的氢氧化钠溶液中逐渐加入稀盐酸至恰好完全反应.溶液的颜色变化是,该反应的化学方程式是.