选考【有机化学基础】
A是一种重要的化工原料,已知A是一种卤代烃相对分子质量为92.5,其核磁共振氢谱中只有一个峰,C是一种高分子化合物,M是一种六元环状酯,转化关系如图所示,回答下列问题: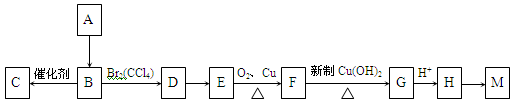
(1)A的分子式为 ;A→B的反应类型 ;
(2)有机物D的结构式为 。 M的结构简式为 。
(3)写出下列反应的化学方程式:
B→C: ;
E→F: 。
(4)写出满足下列条件的H的同分异构体d的结构简式 。
①属于酯类;
②能发生银镜反应;
③能与金属钠反应放出气体。
④核磁共振氢谱有三个峰,且峰面积比为6:1:1
(本小题满分8分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态):
| 时间(min) |
0 |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
0 |
50 |
120 |
232 |
290 |
310 |
(1)哪一段时段的反应速率最快,原因是。
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)。
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)。
(本小题满分8分)乙烯来自石油的重要化工原料,其产量是一个国家石油化工水平的标志。请回答:
(1) (3分)乙烯通入溴的四氯化碳溶液中,观察到的现象是 ;其反应方程式为 ;乙烯在一定条件下发生加聚反应的化学方程式为 。
(2) (3分)此外,乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一: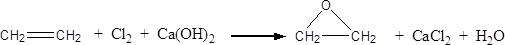
工艺二:
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,因此,在实际生产中,应采用工艺更环保、更经济。
(本小题满分14分)a、b、c、d、e四种短周期元素的原子序数逐渐增大。a为非金属元素,且a、e同主族,c、d为同周期的相邻元素。e原子的质子数等于c、d原子最外层电子数之和。b原子最外层电子数是内层电子数的2倍。c的氢化物分子中有3个共价键。试推断:
(1)写出b元素在周期表中的位置;
(2)有a、c、d所形成的离子化合物是它与e的最高价氧化物对应水化物的溶液加热时反应的离子方程式是;
(3)c的单质的电子式为。
(4)b和d相比,非金属性较强的是(用元素符号表示),下列事实能证明这一结论的是(选填字母序号)。
| A.常温下,b的单质呈固态,d的单质呈气态 |
| B.d的氢化物的稳定性强于b的氢化物 |
| C.b与d形成的化合物中,b呈正价 |
| D.d的氢化物的沸点高于b的氢化物 |
(5)元素b形成的一种单质具有硬度大、熔点高的物理性质,据此判断该单质的晶体类型为。
(本小题满分9分)
(1)把6 mol A气体和5 mol B气体混合放入4 L密闭容器中,在一定条件下发生反应:3A(g)+B(g) 2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
(2)反应2H2(g) + O2(g)= 2H2O(g)的能量变化如图所示。已知拆开1molH2、1molO2和1molH-O中的化学键分别需要消耗436KJ、496KJ和463KJ能量,则该反应(填“吸收” 或“放出”)KJ热量。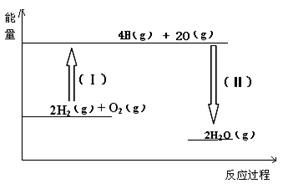
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右图所示:
a、b两个电极均由多孔的碳块组成。写出a极的电极反应式:。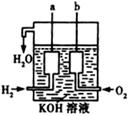
(4)工业上用电解饱和食盐水的方法制取金属氯气,反应中能量的转化形式是;氯气在极上产生,反应后溶液的pH。(填“增大”或“减小”)。
(8分)试用 ══
══ ↑的反应设计原电池。
↑的反应设计原电池。
(1)原电池中使用的电解质溶液是;
(2)写出电极反应式:
负极:,正极;
(3)在方框中画出此原电池的图,标出电极材料的名称。