选考[化学—选修化学与技术]
通常情况下,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,各国都在限制CO2的排量,同时也加强对CO2创新利用的研究。
(1)目前,推广用超临界CO2(介于气态和液态之间)代替氟利昂作致冷剂,这一做法对环境的积极意义是 。
(2)科学家为提取空气中的CO2,把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应使之变为可再生燃料甲醇。流程如图:
①分解池中反应的化学方程式为: 。
②合成塔中,若有4.4g CO2与足量H2恰好反应生成气态产物,放出4.947kJ的热量,写出该反应的热化学方程式: 。
(3)某同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积Ksp分别为4.96×10-9、2.58×10-9。他最好将空气通入足量的 溶液,实验时除测定温度、压强和空气的体积外,还需测定 。
反应
 过程中的能量变化如图所示,回答下列问题。
过程中的能量变化如图所示,回答下列问题。
(1)该反应是反应(填"吸热""放热");
(2)当反应达到平衡时,升高温度,
的转化率(填"增大""减小""不变"),原因是;
(3)反应体系中加入催化剂对反应热是否有影响?,原因是:
(4)在反应体系中加入催化剂,反应速率增大,
和
的变化是:
,
(填"增大""减小、""不变")。
在一个固定体积的密闭容器中,保持一定温度,进行以下反应:H2(g)+Br2(g)  2HBr(g)。已知加入1 mol H2和2 mol Br2时,达到平衡后生成a mol HBr(见下表的“已知”项),在相同条件下,且保持平衡时各组分的含量不变,对下列编号(1)~(3)的状态,填写表中的空白。
2HBr(g)。已知加入1 mol H2和2 mol Br2时,达到平衡后生成a mol HBr(见下表的“已知”项),在相同条件下,且保持平衡时各组分的含量不变,对下列编号(1)~(3)的状态,填写表中的空白。
| 编号 |
起始状态(mol) |
平衡时HBr(g) 物质的量(mol) |
||
| H2 |
Br2 |
HBr |
||
| 已知 |
1 |
2 |
0 |
a |
| (1) |
2 |
4 |
0 |
|
| (2) |
1 |
0.5 a |
||
| (3) |
m |
n(n≥2m) |
、已知可逆反应:
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=" 1" mol,L-1, c(N)="2.4" mol·L-1; 达到平衡后,M的转化率为60%,此时N的转化率为;
(2)若反应温度升高,M的转化率(填“增大”、“减小”或“不变”;)
(3)若反应温度不变,反应物的起始浓度分别为:c(M)= 4mol,L-1, c(N)="a" mol·L-1;达到平衡后,c(P)="2" mol·L-1,a= (要求写出计算过程) ;
(4)若反应温度不变,反应物的起始浓度为:c(M)=" c(N)=b" mol,L-1,达到平衡后,M的转化率为
(要求写出计算过程)。
(14分) 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)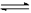 CO(g)+H2O(g),其化
CO(g)+H2O(g),其化
学平衡常数K与温度t的关系如下:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
请回答下列问题:(1)该反应的化学平衡常数K =。
(2)该反应为反应。(填“吸热”或“放热”)
(3)800℃,固定容积的密闭容器中,放入混合物,起始浓度为c(CO)="0.01" mol/L, c(H2O)="0.03" mol/L, c(CO2)="0.01" mol/L, c(H2)="0.05" mol/L ,则反应开始时,H2O的消耗速率比生成速率(填“大”、“小”或“不能确定”)
(4)830℃,在1 L的固定容器的密闭容器中放入2 mol CO2和1 mol H2,平衡后CO2的转化率为, H2的转化率为。
在标准状况下,4g H2,11.2L O2,1mol H2O中,所含分子数最多的是______,含原子数最多的是________,质量最大的是________,体积最小的是________。