化学兴趣小组用下图所示装置进行探究实验。以验证产物中有乙烯生成且乙烯具有不饱和性。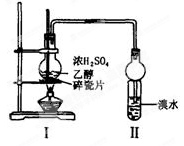
当温度迅速上后,可观察到试管中的溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色。(已知:二溴乙烷密度2.18 g·cm-3,不易溶于水,易溶于醇、醚、丙酮等有机溶剂)。
请回答下列问题:
(1)该实验中生成乙烯的化学方程式:_______________________________________。
(2)甲同学认为:该混合液体反应复杂,溴水褪色的现象不能证明反应中有乙烯生成及乙烯具有不饱和性。下列理由中正确的是 __________(填选项)。
A.乙烯与溴水易发生取代反应
B.使溴水褪色的反应,未必是加成反应
C.使溴水褪色的物质,未必是乙烯
D.浓硫酸氧化乙醇生成乙酸,也会使溴水褪色
(3)乙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加了如下图所示装置。
则A中的试剂应为 ___________,B中的试剂为____________。
(4)丙同学经过观察后认为:试管中另一现象可证明反应中有乙烯生成,这个现象是:___________;为验证这一反应是加成反应而不是取代反应,可用pH试纸来测试反应前后溶液的酸性变化,原理是:_____________________。
(5)处理上述实验后烧瓶中废液,最合理的方法是______________(填选项)。
A.废液经冷却后倒入下水道中
B.废液倒入空废液缸中
C.将水加入烧瓶中稀释后倒入废液缸
D.废液倒入盛有水的塑料桶中,经处理后再倒入下水道
某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
| 实验步骤 |
向3—4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
| 实验现象 |
产生白色沉淀 |
| 离子方程式 |
(1) |
| 小组讨论交流 |
向上述反应后的清液中滴入适量1mol/L的Na2CO3溶液会出现什么现象 |
| 假设出现的实验现象,说明理由 |
假设:Ⅰ无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ(2),理由:(3) |
| 证明你的假设 |
现象:产生大量的白色沉淀 |
| 离子方程式 |
(4) |
| 解释 |
(5) |
某化学兴趣小组为了探究:在常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:;猜想2;猜想3。
为了验证猜测,该小组设计实验加以探究:
[实验探究]
该小组同学按如图所示装置,将气体从a端通入: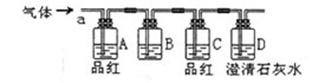
(1)B中应该装下列试剂(填编号);
| A.NaCl溶液 | B.KMnO4溶液 | C.浓溴水 | D.饱和NaHCO3溶液 |
(2)A中品红的作用是:;
(3)D中澄清石灰水的作用是:。
通过该实验,小组同学观察到以下三个实验现象:
①A中品红褪色②C中品红不褪色③D中澄清石灰水变浑浊
[得出结论]
由上述现象小组同学确认该气体的成分是。
实验室用98%的浓硫酸(其密度为1.84 g/ml)配制100 mL
1.0 mol·L-1稀硫酸。
(1)需用10 mL的量筒量取浓硫酸的体积为mL。
(2)实验时选用的仪器有10 mL量筒、烧杯、玻璃棒、、。
(3)配制过程中,下列情况会使配制结果偏低的是(填序号)。
A.用量筒量取浓硫酸时,仰视量筒的刻度
B.转移液体到容量瓶中时,未洗涤烧杯就定容
C.往容量瓶转移时,有少量液体溅出
D.容量瓶使用时未干燥
E.定容时俯视刻度线观察液面
(4)在容量瓶使用方法中,下 列操作正确的是(填序号)。
列操作正确的是(填序号)。
A.容量瓶用蒸馏水洗净后,再用待配液润洗
B.使用容量瓶前检查它是否漏水
C.将氢氧化钠固体放在天 平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.将准确量取的18.4 mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
(4分)下图是实验室制取溴苯的装置:
导管a段的作用。反 应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
1,2—二溴 乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于有机溶剂,在实验室中可以用下图所示装置制备1,2—二溴乙烷。其中分液漏斗和烧瓶a中装有酒精和浓H2SO4的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:
乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于有机溶剂,在实验室中可以用下图所示装置制备1,2—二溴乙烷。其中分液漏斗和烧瓶a中装有酒精和浓H2SO4的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:
(1)写出实验中制备1,2—二溴乙烷的两个化学反应方程式,
。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象。
(3)容器c中NaOH溶液的作用是__________________________________。