工业常用燃料与水蒸气反应制备H2和CO, 再用H2和CO合成甲醇。
(1)制取H2和CO通常采用:C(s)+H2O(g)  CO(g)+H2(g) △H=+131.4 kJ·mol-1,下列判断正确的是 。
CO(g)+H2(g) △H=+131.4 kJ·mol-1,下列判断正确的是 。
a.该反应的反应物总能量小于生成物总能量
b.标准状况下,上述反应生成1L H2气体时吸收131.4 kJ的热量
c.若CO(g)+H2(g) C(s)+H2O(1) △H=-QkJ·mol-1,则Q<131.4
C(s)+H2O(1) △H=-QkJ·mol-1,则Q<131.4
d.若C(s)+CO2(g) 2CO(g) △H1;CO(g)+H2O(g)
2CO(g) △H1;CO(g)+H2O(g) H2(g)+CO2(g) △H2则:△H1+△H2=+131.4 kJ·mol-1
H2(g)+CO2(g) △H2则:△H1+△H2=+131.4 kJ·mol-1
(2)甲烷与水蒸气反应也可以生成H2和CO,该反应为:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
已知在某温度下2L的密闭绝热容器中充入2.00mol甲烷和1.00mol水蒸气,测得的数据如下表:
| |
不同时间各物质的物质的量/mol |
|||
| 0 min |
2min |
4min |
6min |
|
| CH4 |
2.00 |
1.76 |
1.60 |
n2 |
| H2 |
0.00 |
0.72 |
n1 |
1.20 |
根据表中数据计算:
①0 min~2min内H2的平均反应速率为 。
②达平衡时,CH4的转化率为 。在上述平衡体系中再充入2.00mol甲烷和1.00mol水蒸气,达到新平衡时H2的体积分数与原平衡相比 (填“变大”、“变小”或“不变”),可判断该反应达到新平衡状态的标志有______。(填字母)
a.CO的含量保持不变
b.容器中c(CH4)与c(CO)相等
c.容器中混合气体的密度保持不变
d.3ν正(CH4)=ν逆(H2)
(3)合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的。工作原理如下图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过)。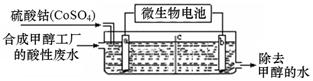
①a电极的名称为 。
②写出除去甲醇的离子方程式 。
③微生物电池是绿色酸性燃料电池,写出该电池正极的电极反应式为 。
现有X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素。有关信息如下表:
| 原子或分子相关信息 |
单质及其化合物相关信息 |
|
| X |
ZX4分子空间结构为正四面体 |
X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y |
Y原子的最外层电子数等于电 |
Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料(人造刚玉) |
| Z |
Z原子的最外层电子数是次外层电子数的 |
Z是无机非金属材料的主角,其单质为原子晶体,是一种优良的半导体材料 |
| W |
W原子的最外层电予数小于4 |
W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1)W位于周期表第四周期第族,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为。
(2)Z最简单的氧化物分子是分了(填“极性”或“非极性”):工业上用Z的氧化物制备其单质的化学反应方程式为。
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它最常用来制造晶体篱,最新研究表明:有机锗具有明显的抗肿瘤活性,锗元素的最高价氧化物的化学式为。
(3)实验室制取X单质的离子方程式为;X的气态氧化物的水溶液与Y的氧化物反应的离子方程式为。
(4)在50mL lmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能为mL或mL。
已知有下图所示物质相互转换关系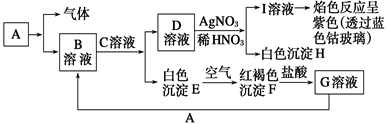
试回答:
(1)写出B的化学式,D的化学式。
(2) 写出由E转变成F的现象;其发生反应的化学方程式________。
写出由E转变成F的现象;其发生反应的化学方程式________。
(3)鉴别B溶液中阳离子的操作方法及实验现象__________________;
(4)向G溶液中加入A的离子方程式________
有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO、CO中的一种或几种,取此溶液做下列实验:①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气 体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断:
体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断: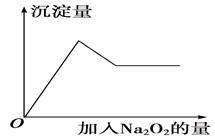
(1)溶液中一定含有的离子是______________ 。
。
(2)溶液中肯定不含有的离子是_______________ _。
_。
(3)可能含有的离子是____________。
A 、B、C、D是四种可溶性化合物,分别由阳离子K+、Ba2+.、Al3+、 Fe3+和阴离子OH—、CO
、B、C、D是四种可溶性化合物,分别由阳离子K+、Ba2+.、Al3+、 Fe3+和阴离子OH—、CO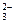 、NO
、NO 、SO
、SO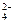 两两组合而成,它们的溶液能发生如下反应:
两两组合而成,它们的溶液能发生如下反应:
(1)A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失。
(2)C与D反应生成有色沉淀。
(3)B与C反应生成白色沉淀。
写出它们的化学式:
A._________;B._________;C._________;D._________;
下图为中学化学中常见物质的转化关系,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物,试推断:
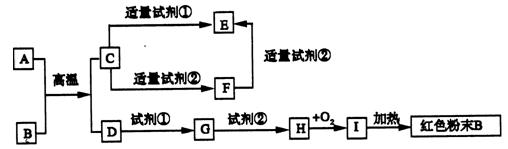
(1)写 出物质的化学式:
出物质的化学式:
(2)写出下列反应的方程式:
C →F的离子方程式:_____________________________________________
→F的离子方程式:_____________________________________________
H→I的化学方程式:______________________________________________