(共10分前2个空每空一个1分,其余每空2分)依据氧化还原反应2Ag+(aq)+Cu(s) ="===" Cu2+(aq)+2Ag(s)设计的原电池如图所示: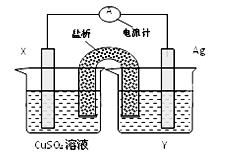
请回答下列问题:
(1)外电路中的电子是从_______ 电极流向________电极。
(2)银电极发生的电极反应为________________________;
X电极上发生的电极反应为___________________________;
(3)LiSOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为4Li+2SOCl2==="4LiCl" +S +SO2↑。请回答下列问题:
写出电池的负极发生的电极反应为_________________________________________;
电池正极发生的电极反应为______________________________________;
C和Si分别是构成生命体和岩石的重要元素。
(1)CH4和SiH4沸点较高的是。原因是。稳定性较高的是。
(2)SiC的晶体结构与晶体硅相似,其中C原子的杂化方式为。微粒间存在的作用力是。
(3)CO2形成的干冰晶体与SiO2晶体相比,下列说法不正确的有。
A中心原子的杂化方式不同B构成晶体的微粒种类不同 C晶体内微粒间作用力不同
D晶体导电性不同 E.常温时,晶体挥发性不同
(4)已知键能数据如下,化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。写出Si(s)在O2中燃烧生成SiO2(s)的热化学方程式。
| 化学键 |
Si—O |
O=O |
Si—Si |
| 键能(kJ·mol-1) |
460 |
498 |
226 |
(5)氨基酸是构成蛋白质的物质基础,甘氨酸H2N-CH2-COOH中,各元素的电负性从大到小为。
选择以下物质填写下列空白:
| A.氢氧化钠 | B.氧化镁 | C.He | D.二氧化硅 |
E.氯化铵 F.碘晶体 G.二氧化硫 H.钾
(1)晶体中存在分子的是。(2)晶体中既有离子键又有共价键的是。
(3)融化时需要破坏共价键的是。(4)最易溶于水的分子晶体是。
已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E。又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的。D原子得到一个电子后其3p轨道将全充满。B+离子比D原子形成的离子少一个电子层。C与B可形成BC型的离子化合物。E的原子序数为29。
请回答下列问题:
(1) 元素A简单氢化物中A原子的杂化类型是,B、C、D的电负性由小到大的顺序为
__(用所对应的元素符号表示)。C的气态氢化物易溶于水的原因是。
(2)E原子的基态电子排布式为。元素E的单质晶体在不同温度下可有两种堆积方式,晶胞分别如右图a和b所示,则其面心立方堆积的晶胞与体心立方堆积的晶胞中实际含有的E原子的个数之比为。
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 |
NaCl |
KCl |
CaO |
| 晶格能/kJ·mol-1 |
786 |
715 |
3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是。
(15分)碳和氮的化合物与人类生产、生活密切相关。
(1)在一恒温、恒容密闭容器中发生反应: Ni(s)+4CO(g)  Ni(CO)4(g),
Ni(CO)4(g), H<0。利用该反应可以将粗镍转化为纯度达99.9%的高纯镍。对该反应的说法正确的是
H<0。利用该反应可以将粗镍转化为纯度达99.9%的高纯镍。对该反应的说法正确的是
(填字母编号)。
| A.增加Ni的量可提高CO的转化率,Ni的转化率降低 |
B.缩小容器容积,平衡右移, H减小 H减小 |
| C.反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低 |
| D.当4vNi(CO)4=v(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态 |
(2)CO与镍反应会造成镍催化剂中毒。为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫。
已知:C(s)+ O2(g)==CO(g)
O2(g)==CO(g) H= -Q1 kJ·mol-1
H= -Q1 kJ·mol-1
C(s)+ O2(g)==CO2(g) H= -Q2 kJ·mol-1
H= -Q2 kJ·mol-1
S(s)+O2(g)==SO2(g) H= -Q3 KJ·mol-1
H= -Q3 KJ·mol-1
则SO2(g)+2CO(g)==S(s)+2CO2(g) H=kJ·mol-1。
H=kJ·mol-1。
(3)金属氧化物可被一氧化碳还原生成金属单质和二氧化碳。图(1)是四种金属氧化物(Cr2O3、SnO2、PbO2、Cu2O)被一氧化碳还原时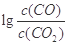 与温度(t)的关系曲线图。
与温度(t)的关系曲线图。
700oC时,其中最难被还原的金属氧化物是(填化学式),用一氧化碳还原该金属氧化物时,若反应方程式系数为最简整数比,该反应的平衡常数(K)数值等于 。
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如上图(2)所示。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为。
若该燃料电池使用一段时间后,共收集到20mol Y,则理论上需要消耗标准状况下氧气的体积为L。
【化学—--选修3:物质结构与性质】
金属铜与金属锰及其化合物在工业上有着广泛的应用:
(1)Cu2+的外围电子排布图可表示为;
(2)Mn基态原子核外处在能量最高的能级上的电子共有种不同的运动状态;
(3)在铜锰氧化物的催化下,空气中CO被氧化成CO2,HCHO被氧化成CO2和H2O
① N3-和CO2是等电子体,则N3-的结构式为;
② HCHO分子中C原子轨道的杂化类型为;
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为;
(5) 用晶体的x射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm(提示:3.613=47.05),又知铜的密度为9.00g·cm-3,则铜晶胞的质量是
g(保留两位小数);阿伏加德罗常数为(列式计算,保留两位小数)。