某兴趣小组利用下图装置(省略夹持仪器)探究二氧化碳与氢氧化钠溶液的反应。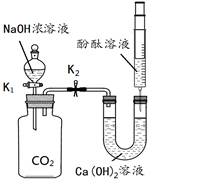
【实验步骤】
①将足量的氢氧化钠浓溶液装入分液漏斗中。
②打开止水夹K 1,待氢氧化钠浓溶液完全进入广口瓶之后立即关闭K1。
③待充分反应后,打开止水夹K2。
【实验现象】
整个实验过程中,观察到注射器中的液体________,U型管中________,广口瓶中的液体出现浑浊。
【实验解释】
步骤②中发生反应的化学方程式为________。产生上述现象的原因是__________。
某实验小组将制作皮蛋的原料生石灰、纯碱和食盐放入水中,充分反应后过滤,得到澄清溶液。对该溶液的组成,甲、乙同学分别做出以下推测:
(1)我认为上述两位同学的推测都有不足,甲同学推测错误的原因是_________________;乙同学推测错误的原因是。
(2)我的推测是:该溶液中一定存在的溶质是_________________。为进一步确定该溶液可能的组成,甲、乙同学设计了如下实验进行探究,
| 实验操作 (填所加试剂的化学式) |
实验现象 |
实验结论 |
该溶液的组成 |
 |
有气泡生成 |
有Na2CO3 |
|
 |
有沉淀生成 |
有Ca(OH)2 |
小丽同学在刚买来的袋装薯片中发现还有一个小袋,上面标有“成分:CaO、Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末有少许是棕红色,大多数是灰白色的。经过分析,她认为棕红色粉末是Fe2O3,灰白色粉末应该含有CaCO3和Fe,为验证自己的判断,小丽同学打算进行实验探究,请你一同参与。
【实验目的】证实灰白色粉末中含有CaCO3和Fe。
【实验设计】装置如下图所示:
【实验预测与分析】
①若要证实样品中含有CaCO3,观察到的实验现象是,B中发生反应的化学方程式为。
②若要证实样品中含有Fe,D中应该观察到的现象是,E中白色硫酸铜粉末变蓝,此时C装置的作用是
③看了小丽同学的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,请你写出其中一种物质的化学式。
丹丹同学发现妈妈做包子、馒头时,向面团中加入发酵粉,蒸出的包子、馒头中有许多小孔,松软可口,丹丹同学对发酵粉产生了兴趣。
⑴提出问题:发酵粉的主要成分是什么物质?
⑵查阅资料:含钠元素的物质在酒精灯的火焰上灼烧时,会产生黄色火焰。
⑶实验探究:下面是丹丹同学设计的探究实验,请你帮她完成。
①将发酵粉取样,在酒精灯的火焰上灼烧产生黄色火焰。
②取样于试管中,加入稀盐酸,产生大量的气泡,将该气体通入澄清石灰水,澄清的石灰水变浑浊,则发酵粉的主要成分中含有的离子是(写离子符号)。
⑷小结与思考:
①发酵粉的主要成分是(写化学式)。
②发酵粉与面粉、水混合发酵产生CO2气体,这些气体会在面团中形成许多小孔,使包子、馒头松软可口。
③实验室制取CO2可选择下列装置中的(填字母序号)。
④实验室用A装置制取氧气的化学方程式为。用F装置收集氧气时,还可用于测定氧气的体积,此时还需要(填仪器名称),氧气由(填序号)进入F中。
(14分)某同学为了研究酒精的性质,做了如下探究,请你把他的探究情况完成。
(1)通过观察酒精灯内的酒精,酒精的颜色是__________,状态__________;
(2)闻闻它的气味,酒精___________气味;
(3)用滴管吸取一些酒精滴入盛有少量水的试管中,可见酒精_(“溶”或“不溶”)于水;
(4)用火柴点燃酒精灯,然后把干燥的冷烧杯罩在酒精灯的火焰上方,发现烧杯内壁__________,把烧杯倒立过来立即注入少量澄清石灰水,振荡后发现石灰水_______,通过这两个现象说明酒精燃烧时生成水和二氧化碳,该反应的文字表达式为。
有人喜欢中凌晨天刚朦朦亮时到公园中锻炼身体,这种方法对人体好吗?雨辰同学认为对人体有利,因为凌晨空气清新;周洁认为对人体有害,因为凌晨森林公园中空气中的二氧化碳的含量太高,对人体有害,应该等日照以后再进入其中进行锻炼。根据你学的知识判断,你认为的观点是正确的。为了研究凌晨森林公园空气中的二氧化碳和氧气的含量与日照后森林公园中二氧化碳和氧气含量的关系。他们设计了如下实验:
(1)分别收集凌晨森林公园中空气和日照后公园中的空气各一瓶到实验室。收集日照后公园中空气的方法是。
(2)为比较两瓶气体中二氧化碳含量的高低,你采用的实验方案是。预期的实验现象是。由此得出的结论是。